Weekly COVID-19 Review 20200522
4월말 백악관에서 Operation Warp Speed를 언급했을 때부터 이제는 백신으로 포커스가 바뀌었고, 4월까지 렘데시비어가 주식시장에서 했던 역할을 이제는 백신이 대신 할거라고 말씀드려왔습니다. 대략 시기는 6월 이후 부터라고 봤는데 모더나가 임상 결과를 예상보다 일찍 발표하면서 그 시기도 앞당겨 졌네요.
같이 뽐뿌질 해줄만한 치료제 후보물질이 클로로퀸 이외에는 없다시피했던 렘데시비어와는 달리 백신의 경우 모더나 말고도 10여종의 백신이 임상시험에 진입해 있습니다. 이중 미국 시장에 영향이 크지 않을 중국발 백신 5종을 제외하면 나머지 5종의 임상시험 결과들이 6월경부터 차례로 나오게 될 예정입니다.
미국의 하루 확진자 수가 여전히 2만명대를 기록하고 있고, 일찍 reopening을 시작한 주들에서 확진자수가 다시 증가하고 있습니다. 미국의 50개주 전부가 이제는 reopening을 하는 상황인 만큼 2차 웨이브는 피할 수 없을 것 같습니다. 백신 개발에 대한 관심은 계속 증가하게 될 것이고 시장에 대한 파급력도 커질 것 같습니다.
▶Weekly Biotech Review 20200522
※ 리뷰 내용중 사실관계가 잘못됐거나, 해석의 오류가 있거나, 간단히 제시한 필자 의견에 이견이 있거나, 혹은 잘 이해가 안가거나, 궁금한 내용이나 제안이 있으신 분들은 언제든 댓글로 알려주시기 바랍니다. 포스팅이 도움이 되시면 “공감”을 눌러주시면 포스팅 작성하는데 많은 힘이 됩니다.
진단
진단 관련 기업들은 이제 숫자로 실적을 보여줘야할 때가 됐습니다. 이전처럼 단순히 테스트를 개발했다, 출시했다와 같은 이슈로는 주가가 움직이기 어려워 보입니다. 다만 가정용 키트와 타액 채취 처럼 비강 스왑보다 덜 침습적이고 전문인의 손길이 필요없는 간편한 샘플 채취방식에 대한 수요는 계속 있을듯 하니 관련 이슈를 보시는 것이 좋을 것 같습니다. 더불어 아직은 큰 이슈는 아니지만 소아 다기관 염증 증후군 (multisystem inflammatory syndrome in children, MIS-C)의 진단법 (및 치료제)에 대해서도 계속 주시하고 있는 것이 좋을 듯 합니다.
[핵산 진단]
Fulgent Genetics (NASDAQ:FLGT): FDA가 Everlywell의 여러 COVID-19 테스트에서 사용가능한 범용 가정용 샘플 채취 키트 COVID-19 Test Home Collection Kit에 대해 EUA 발급. 가정용 샘플 채취 키트로는 최초. 가정에서 키트를 이용 비강 스왑 샘플을 채취해 허가된 랩에 보내 검사 받는 방식. 채취된 샘플에 대한 테스트는 Assurance Scientific Laboratories와 Fulgent Genetics에서 담당.
Thermo Fisher Scientific (NYSE:TMO): 미국 연방정부가 Thermo의 viral transport media (VTM, 비강 스왑으로 채취한 샘플을 녹여내는 용액)에 대해 수주 계약. Thermo는 캔자스 주 Lenexa 공장에 300명을 신규 고용해서 주당 생산량을 50K에서 1M으로 증산할 예정.
Quidel (OTC:QDEL): RNA 추출과정이 생략된 Lyra Direct SARS-CoV-2 Assay에 대해 FDA의 EUA와 EC의 CE마크를 받았다고 발표.
GlaxoSmithKline (GSK): Mammoth Biosciences와 CRSPR-Cas12를 이용해서 SARS-CoV-2를 검출하는 DETECTR 진단법 개발에 대한 협업 계약을 체결. CRSPR-Cas12를 이용한 진단법은 20분만에 검출 가능하면서 PCR 기반 테스트와 유사한 정도의 민감도와 특이도를 보이고, 무엇보다도 핵산 진단법이면서도 비용이 저렴하고 사용법이 간단해서 OTC로도 사용이 가능하다는 장점이 있음. 성공적으로 개발될 경우 코로나-19뿐만 아니라 일반적인 핵산 진단 시장의 판도를 바꿀만한 포텐셜이 있다는 평가. Mammoth Biosciences는 CRISPR Therapeutics (CRSP)의 설립자인 UC Berkely의 Jennifer Doudna 교수가 설립한 크리스퍼를 이용한 진단법을 개발하는 비상장 기업.
Abbott (NYSE:ABT): 지난주 NYU에서 처참한 민감도를 발표해 논란이 일었던 신속 핵산 진단 ID Now에 대해 여러 urgent care clinics에서 진행중인 임상시험의 중간 결과를 공개. Roche의 cobas SARS-CoV-2와의 비교에서는 29명의 양성 환자 모두와 음성환자 227명 중 226명에 대해 일치하게 진단. CDC의 Novel Coronavirus (COVID-19)와의 비교에서는 94.7%의 민감도와 98.6%의 특이도를 보임.
OraSure Technologies (NASDAQ:OSUR): FDA가 가정용 타액 샘플 수집기기 OMNIgene ORAL (OM-505)와 P23 Labs의 TaqPath SARS-CoV-2 진단 테스트에 대해 EUA 발급.
▶EUA로 승인된 핵산진단법들의 민감도 비교 (4월2일자)
[항체 진단]
※ FDA가 항체 테스트에 대해 제시한 기준은 PCR 테스트와 비교하여 90% 이상의 PPA와 95% 이상의 NPA를, IgG와 IgM을 나눠서 하는 경우에는 PPA 각각 90%, 70% 이상. FDA는 기준 제시를 위해 일반적으로 사용되는 민감도 (sensitivity)와 특이도(specificity) 대신 새로운 개념인 PPA (positive percent agreement)과 NPA (negative percent agreement)라는 개념을 도입했는데 결국은 같은 개념. Sensitivity/PPA는 위양성률 – 핵산 테스트 양성 확진자를 음성으로 판단하는 비율, specificity/NPA는 위음성률 – 핵산 테스트 음성 판정자를 양성으로 판정하는 비율을 뜻함. 항체 테스트를 직장 복귀의 수단으로 이용하려고 하는 마당이라 위음성률이 더 중요한 요소. 항체 테스트는 노이즈가 많아 일반적으로 위음성율이 좋지 않음.
※ Valdiation이란 GLP, CLIA 등의 보증된 랩 (certified lab)에서 진단 키트가 정해진 기간, 정해진 환경에서 반복적으로 동일한 결과를 낼 수 있음을 검증하는 과정이라고 이해하면 됨.
Becton Dickinson (NYSE:BDX): FDA가 2주전 예고한대로 제시한 기준에 미달한 항체 테스트 28종을 FDA의 리스트에서 제외시킴. 이 28종은 미국에서 더이상 판매할 수 없음. 이중 절반 이상은 중국 제품이지만 Becton Dickinson을 통해 유통되는 BioMedomics의 제품도 포함. BioMedomics는 시장에서 자진 철수. 28종의 테스트중 EUA를 받은 제품은 없음. FDA는 최근 2주간 항체 테스트에 대한 EUA 발급이 없는 상태. 더불어 이 리스트는 계속 업데이트 될 예정이라고 해서 시장에서 퇴출되는 항체 테스트는 더 늘어날 것임을 예고.
Chembio Diagnostics (NASDAQ:CEMI), Thermo Fisher Scientific (NYSE:TMO): 신속 IgM/IgG 항체 혈액 테스트인 Chembio의 DPP COVID-19 System의 미국내 유통을 Thermo Fisher가 담당하기로 계약.
Alphabet (NASDAQ:GOOG, GOOGL): 알파벳의 생명과학 자회사 Verily가 임상시험 데이타 분석 기술 Project Baseline을 COVID-19에 적용해서 항체 테스트에 대해 연구하기로 했다고 발표.
[기타 진단]
Genetic Technologies Limited (NASDAQ:GENE): 1500명의 COVID-19 환자의 유전체를 분석해서 병원 입원이 필요한 사람과 아닌 사람의 유전자 리스크 분석에 대한 프로토타입 리스크 테스트 개발을 마쳤고 더 많은 수의 환자 유전체를 분석해 리스크 테스트를 확인, 보완한 후 약 30일 후 CLIA 등록을 할 예정이라고 발표. COVID-19 리스크에 대한 유전자 검사로는 최초인듯.
Emergency Use Authorizations
This page lists current Emergency Use Authorizations that make available medical devices to diagnose and respond to public health emergencies.
www.fda.gov
항바이러스 치료제
코로나-19에 대한 의약품 개발은 크게 치료제와 백신으로 나눌 수 있고, 치료제는 다시 항바이러스제와 면역억제제로 나눠서 개발이 진행중입니다. 항바이러스제는 말그대로 바이러스 자체를 타게팅해서 바이러스의 세포 침투, 증식, 복제 등을 막아주는 의약품들입니다.
한편 치료제는 기존에 사용되어왔던 의약품, 다른 적응증으로 이미 개발에 들어가있던 후보물질들에 대한 적응증 변경 물질들과 신규 개발하는 물질들로도 분류할 수 있습니다.
적응증 변경 물질들은 이미 안전성 검사를 마쳤기 때문에 곧바로 후기 임상시험에 들어갈 수 있어서 판데믹 초기에 각광을 받은 물질들인 Gilead Sciences의 Veklury (remdesivir), Taisho/Fujifilm의 flu 치료제 Avigan (favipiravir), AbbVie의 HIV 치료제 Kaletra (lopinavir/ritonavir), Bayer의 말라리아 치료제 chloroquine 등이 적응증을 변경한 항바이러스제 후보물질들입니다.
한편 회복된 환자의 피에서 분리한 항체, 새로 발견한 항체, 회복된 환자의 혈청 치료 (Convalescent Plasma) 등은 모두 기존에는 존재하지 않았던 신규 개발하는 항바이러스제입니다. 혈청 치료/혈청에서 분리한 항체 치료와 단일 클론 항체 치료는 본질적으로 바이러스에 결합하는 항체를 이용한 바이러스 중성화가 목적이라는 점에서 동일합니다. 하지만 단일 클론 항체는 항체 유전자를 분석, 클로닝해서 동일한 항체를 대량으로 생산해내는 것이 가능하지만 개발과 생산에 시간이 필요하고, 혈청 치료/혈청에서 분리한 항체 치료는 바로 사용 가능하지만 혈액 공여자가 제공한 혈액 만큼만 사용이 가능하고, 공여자에 따라 서로 다른 항체가 제공된다는 점에서 차이가 있습니다.
코로나-19 감염이 후기로 가면서 급성 폐렴 증상에 의해 환자가 사망에까지 이르게 되는데 이는 바이러스 감염 자체에 의한 증상이라기 보다는 바이러스에 대항하기 위해 과도하게 활성화된 환자의 면역체계가 되면서 환자 자신의 장기를 공격해서 발생하는 사이토카인 스톰이 주 원인일 것으로 추정되고 있습니다. 이에 대해 다양한 면역 억제제들이 임상시험에 돌입해 있는데 대부분이 적응증 변경 의약품들이고 원 적응증은 관절염 등 면역관련 질환인 경우가 많습니다. 최근에는 다양한 세포치료제들이 적은 수의 임상시험이나 compassionate use에서 면역 억제에 좋은 효과를 보인다는 결과도 나오고 있습니다.
최근에는 위에 제시한 일반적인 의약품 작용기제를 벗어나 아무 후보물질이나 일단 효과가 있는지를 테스트해보고자 하는 기조가 보입니다. 가령 COVID-19와는 전혀 무관해 보이는 당뇨병 약이나 항암제 등 테스트해보겠다는건데 이러다가는 설사약도 써보겠다고 나올지도 모르겠습니다. 마이크로캡 바이오텍들의 경우 개발중이던 후보물질을 COVID-19에 테스트해보겠다고 발표하는 것만으로도 주가 부양 효과는 충분히 볼 듯 합니다. 아무리 지푸라기라도 잡는 심정이라지만 옥석은 가려야겠죠.
이상은 치료제의 구분이고 치료제는 이미 감염된 환자들을 치료하는 물질들인 반면, 백신은 비감염자가 감염되지 않도록 바이러스에 대한 항체를 미리 형성하도록 해주는 물질입니다. 하지만 치료제가 예방효과가 있는 경우도 있고, 백신이 치료효과가 있는 경우도 있어서 칼로 무자르듯이 갈리지는 않습니다.
아래 그림은 BioCentury에서 가져온 그림인데 현재 치료제들이 어디를 타겟해서 개발하고 있는지를 잘 보여줍니다. 정리가 잘 되있는 그림이라 계속 포스팅에 포함시킬 예정입니다.

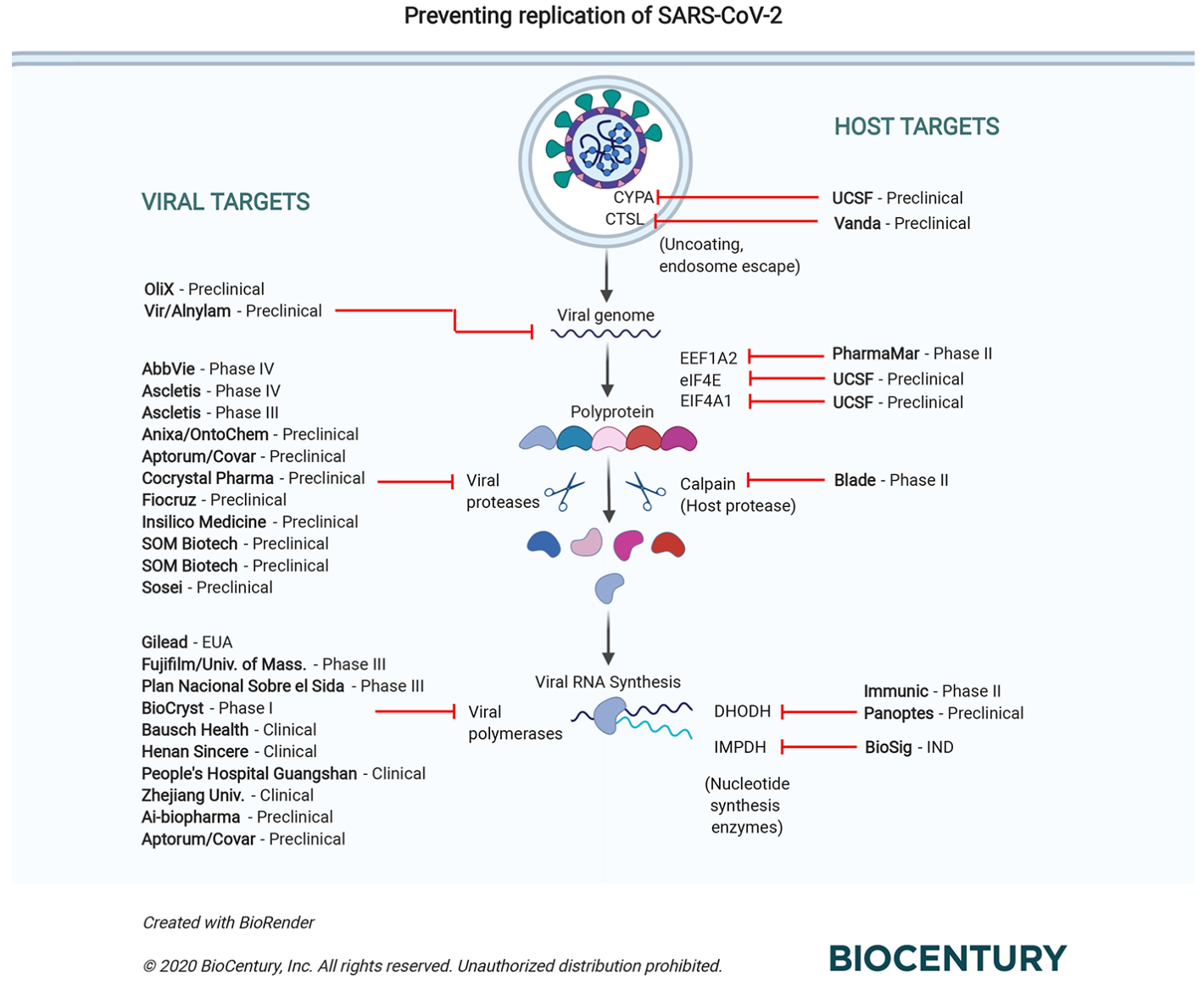
[Remdesivir (Veklury)]
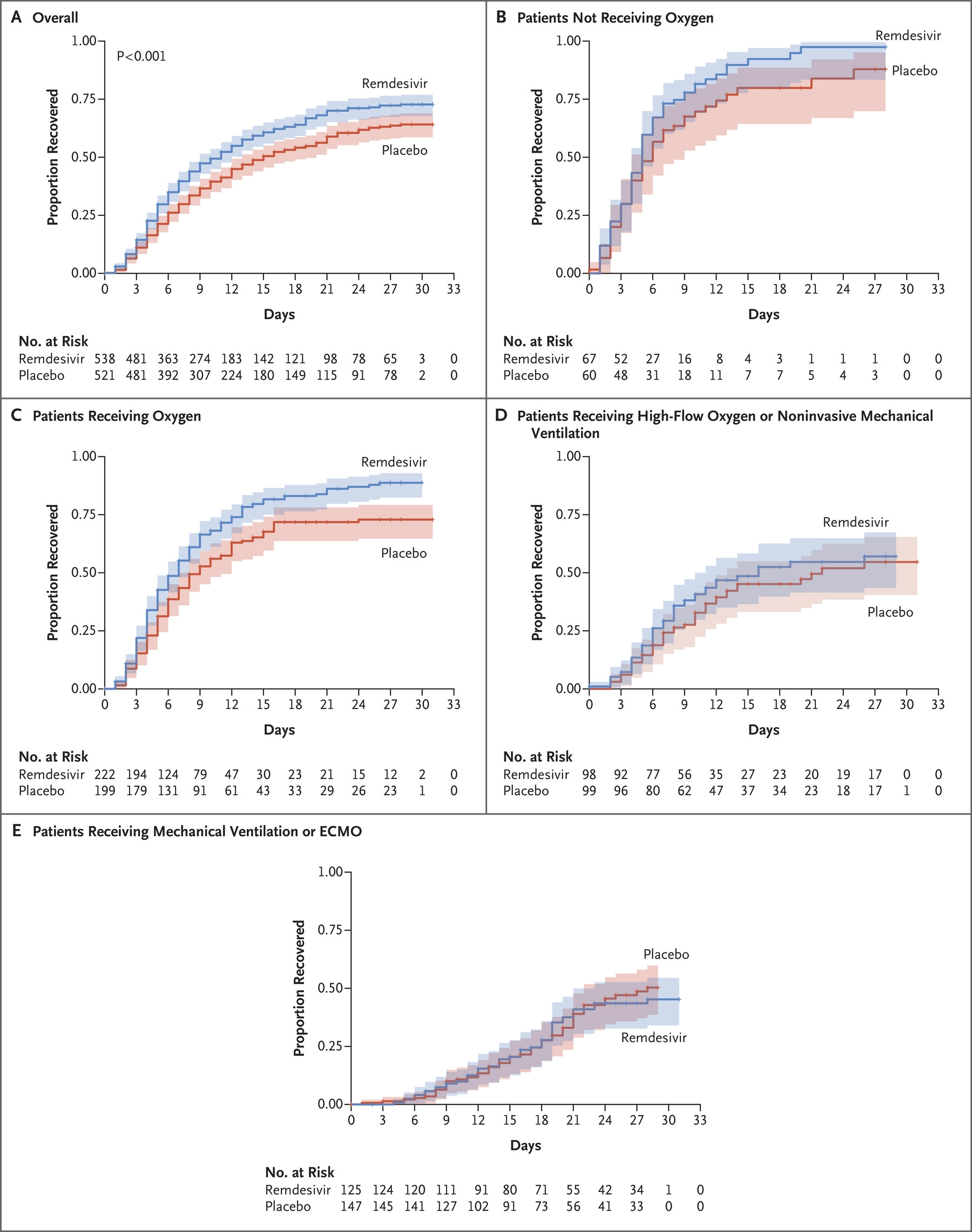
Gilead Sciences (NASDAQ:GILD): 지난 4/29 보도자료로 공개됐던 NIAID 스폰서의 중증 COVID-19 환자에 대한 remdesivir의 임상3상 잠정 결과가 의학전문지 NEJM에 발표. 이전 발표대로 렘데시비어 투여군이 플라시보 대비 더 빠른 회복을 보였고 (중간 회복일 11일 vs 15일) 생존율도 높았음 (14일차 사망율 7.1% vs 11.9%). 그러나 환자의 중증 정도에 따라 산소호흡이 필요없는 환자 (ordinal score 4, not receiving oxygen), 산소 보조장치 환자 (ordinal score 5, receiving oxygen), 비침습 기계 호흡기 환자 (ordinal score 6), receiving high-flow oxygen or noninvasive mechanical ventilation, 에크모 환자 (ordinal score 7, receiving mechanical ventilation or ECMO)으로 나누어 분석했을 때 치료효과는 비교적 경증인 산소호흡이 필요 없거나 산소 보조장치 환자에서만 나타났음 (아래 그림).
NIAID는 좀더 중증 환자들의 경우 환자수가 많지 않아 통계처리시 95% 신뢰구간 (CI)가 너무 넓게 나오는 바람에 나온 결과라고 주장. 일단 통계처리 뒤로하고 수치로만 보자면 초기에 치료할 수록 효과가 잘 나오는게 맞는듯하니 기존에 알려진대로 항바이러스제는 폐병이 너무 심해지기 전에 써야 효과가 있는 듯. 더불어 아직 발표되지 않은 경증-중등증 환자에 대한 임상결과는 잘 나올 듯 보임.
한편 NIAID는 여전히 사망률이 7.1%가 나오기 때문에 다른 의약품과의 병용 테스트가 필요하다고 밝힘. 폐병에 대해서는 ARDS 치료제들이 많이 개발되고 있는데 3주전 NIAID는 이미 렘데시비어와 Lilly의 관절염 치료제 Olumiant (JAK 저해제)를 병용으로 임상시험 한다고 발표했음. ARDS 치료제에 대해서는 아랫쪽 ARDS 섹션 참조 바람.
한편 EU에서 렘데시비어를 조만간 승인한다고 EMA 수장 Guido Rasi이 밝혔음. 주초에 나온 보도인데 아직 승인 발표는 없었는 듯.
[Convalescent Plasma]
※ Convalescent Plasma: 회복된 환자의 혈액에서 분리한 혈장 혹은 그 혈장 내 항체를 이용한 치료
ADMA Biologics (NASDAQ:ADMA): 자회사 ADMA BioCenters Georgia가 convalescent plasma의 수집을 시작했다고 발표. ADMA BioCenters Georgia는 미국 시장에 convalescent plasma를 공급하기로 발표한 6개 회사중 하나.
[기타 항바이러스제]
Vir Biotechnology (NASDAQ:VIR), GlaxoSmithKline (NYSE:GSK): 2003년 SARS에서 회복된 환자에서 추출한 중화항체 S309에 대해 과학 전문지 Nature에 발표. S309는 SARS 뿐만 아니라 SARS-CoV-2에 대해서도 중화작용을 보임. Vir와 GSK는 공동으로 S309와 더불어 VIR-7831, VIR-7832를 COVID-19에 대해 개발 중. Vir는 COVID-19에 대해 가장 폭넓은 포트폴리오로 접근하고 있는 기업임. CEO는 예전 바이오젠 CEO였던 George Scangos. 지금은 COVID-19 테마주이지만 아주 X잡주 바이오텍은 아니니 혹시 물려도 오래 가져갈 기업으로 나쁘지 않음. 관심있는 분들은 한번 공부해 보시길. 필자 블로그에서만 검색해봐도 COVID-19에 대해 어떤 어떤 접근을 하고 있는지 알 수 있음. 언제 기회되면 한번 Vir의 COVID-19 포트폴리오를 따로 뽑아 정리해볼 생각. 사실 주가 폭등은 X잡주들이 훨씬 크겠지만, 이런 애들은 잘못해서 한번 물리면 답 없음. Weekly COVID-19 Review에 실리는 상당수의 종목들이 X잡주들임. 절대 추천 아니고 정보공유 차원이니 알아서 판단하길 바람.
Vir Biotechnology의 간단한 설명은 링크 IPO란 참조
CytoDyn (OTC:CYDY): 멕시코 NIH와 공동으로 중증/위중 COVID-19 환자에 대한 leronlimab의 임상시험을 시작하기로 합의.
Aldeyra Therapeutics (NASDAQ:ALDX): 컨퍼런스콜을 통해 항암제로 개발중이던 HSP90 저헤제 ADX-1612 (ganetespib)이 remdesivir 대비 in vitro에서 더 강력한 항바이러스 작용을 한다고 발표. COVID-19에 대하여 3분기에 FDA에 IND 제출 예정. 또한 염증질환 치료제 후보물질 ADX-629이 cytokine storm에 대해 전임상 단계에서 효과를 보였고 COVID-19환자의 ARDS에 대한 IND는 6월내로 제출 예정이라고 밝힘.
Sorrento Therapeutics, Inc. (NASDAQ:SRNE): Hindenburg Research가 과거 Sorrento 직원 및 전문가들의 말을 인용, 지난주 치료제를 발견했다고 발표한 Sorrento를 비판. 더불어 지난주 발표 이전에 Sorrento는 심각한 자금난과 부채 상환 문제에 직면해 있었다고 하면서 주가 조작에 대한 의문을 제기. 필자의 Sorrento 급등에 대한 뷰는 지난주 Weekly COVID-19 Review 참조 바람.
Atossa Therapeutics (ATOS): 세포 배양 시스템 VERO에서 자사의 AT-H201이 remdesivir 대비 최소 네배, 말라리아약 hydroxychloroquine 대비 최소 20배의 항바이러스 효능을 보인다고 발표. AT-H201은 바이러스의 세포 표면 결합을 막아 세포 감염을 막는 기제라고 설명.
NanoViricides (NYSEMKT:NNVC): SARS-CoV-2 대신 hCoV-NL63 바이러스를 이용해서 동물 모델을 만드는데 성공했고 이 모델을 이용해서 remedesivir 보다 뛰어난 다섯개의 후보물질을 발견했다고 발표. SARS-CoV-2를 사용하는 경우 BSL4에서 실험을 해야하지만 hCoV-NL63를 사용하는 경우 BSL2에서 실험이 가능. BSL4 (위)와 2(아래)의 차이는 아래 사진만 봐도 직관적으로 구분이 가능함. 실제 BSL2는 아래 사진에서 보는 것다 훨씬 널럴함. 그냥 아무 실험실에 사진에 보이는 aseptic hood만 설치하면 됨. BSL4는 아래 사진에서 보듯 우주복에 연결된 해괴한 장비들과 방 자체가 음압으로 되어있고 중간에 옷갈아입고 소독하는 클린룸이 있음. 필자도 직접 본 적 없음.


Cytokine Storm/ARDS 치료제
※ Cytokine Storm: 병원균 등에 의해 촉발된 과도한 면역작용에 의해 면역 시스템이 환자 자신의 기관을 공격하는 증상. 세포치료 항암제 CAR-T에서 주로 발견되는 부작용으로 관심을 받음.
※ ARDS (Acute Respiratory Distress Syndrome): 급성호흡곤란증후군. COVID-19의 주 사망원인이며 Cytokine Storm과 연관되어 있을 것으로 추정.
Amarin Corporation plc (NASDAQ:AMRN): HLS Therapeutics와 공동으로 Vascepa가 COVID-19 환자의 염증 바이오마커에 어떤 영향을 미치는지에 대해 캐나다에서 100명을 대상으로 임상시험을 진행한다고 발표. Vascepa는 오메가-3의 주 성분인 EPA와 DHA중 EPA만 분리해낸 고지혈증/심혈관질환 예방 치료제
[세포치료제]
NantKwest (NK): FDA가 동종이계 중간엽 줄기세포 (allogeneic mesenchymal stem cell, MSC) 치료제 후보물질 BM-Allo.MSC의 COVID-19 환자의 ARDS에 대한 임상 1b상의 IND를 허가.
백신
AstraZeneca (NYSE:AZN): 영국 옥스포드 대학에서 개발중인 ChAdOx1 nCoV-19를 라이선싱한 AstraZeneca가 영국에 9월까지 3천만 도즈, 2020년내에 1억 도즈를 공급하겠다고 밝힘. 또한 미국 보건복지부 산하 BARDA로부터 $1B의 자금지원을 받았으며 미국에 4억 도즈를 공급하겠다고 CEO Pascal Soriot이 블룸버그와의 인터뷰에서 밝힘. 총 생산 캐파는 2021년까지 10억 도즈라고 함.
지난달 임상 1/2상을 시작했고 5월말/6월초에 데이타가 나올 것으로 기대. 또한 임상 3상은 9월에 시작 예정. 지난번 사노피 CEO가 미국에 우선 예약 판매를 하겠다고 하니 프랑스놈들이 난리를 피운걸 본 AstraZeneca는 머리를 좀 쓴 듯. 영국에 준다고 먼저 발표하고 그뒤에 미국에 더 많은 양을 주겠다고 발표.
어느 회사/연구소에서 백신을 먼저 만들지는 모르겠지만 그 백신이 전 세계에 공평하게 분배되리라고 생각하는 것은 아주 나이브한 생각임. 하물며 같은 나라 안에서도 누가 먼저 맞을건지에 대해 논란이 있을 것임. 유심히 안봐서 그런지 한국에서의 백신 개발은 Inovio 얘기 밖에는 못 본 것 같은데, 아무리 CEO가 한국계 미국인라고 해도 결국 미국인이고, Inovio는 미국 회사임. 한국에서도 자체 백신 개발을 했으면 하는 바램.
어쨌건.. 임상시험을 모더나보다 나중에 시작했지만 ChAdOx1 nCoV-19는 한번의 접종만으로 면역효과를 내도록 디자인되었기 때문에 4주 간격으로 두번 접종을 해야하는 모더나보다 진도가 빠를 수 있음. 임상 2상은 70세 이상 및 5세 이상 어린이 포함 현재 자원자 모집중.
지난주 위클리 리뷰에서 빼먹었는데 옥스포드에서 bioRxiv에 원숭이 접종 데이타를 발표했음. 백신을 접종한 원숭이는 바이러스를 감염시켜도 폐병도 안났고, 백신의 가장 큰 문제점인 ADE (antibody-dependent enhancement)도 보이지 않았음 (이거 아주 중요함).
Moderna (NASDAQ:MRNA): NIAID에서 스폰서하는 mRNA-1273 백신 후보물질의 임상 1상 결과 발표. 45명의 15-55세 건강한 성인 대상 25, 100, 250ug을 근육접종으로 28일 간격으로 두번 접종한 결과 첫번째 접종 15일 후 모든 대상자에서 항체가 검출됐고 43일차, 즉 두번째 접종 2주 후 25ug 접종군에서는 회복된 환자에서 발견되는 것과 비슷한 수준의 항체가, 100ug 접종군에서는 이보다 높은 수준의 항체가 검출됐음. 250Ug 접종군에 대해서는 언급이 없는데, 첫 환자 접종이 3/16이고 낮은 용량부터 부작용이 없는지 확인해 가면서 용량을 올리기 때문에 가장 늦게 접종하는 250ug 접종군의 43일차 데이타는 발표당시 아직 없었던 것으로 보임 (설마 있는데 발표 안하는 양아치 짓은 안했을 것으로..). 중화항체의 경우 데이타가 있는 8명 모두 (25ug 4명, 100ug 4명)에서 검출됨. 한국언론에서 18% (8/45)에 불과하다고 하는 걸 여럿 봤는데 100%임 (8/8). 나머지 37명은 ‘아직 모름’임.
중화항체 데이타가 부족한 이유는… 결합 항체의 경우 항원으로 사용한 Spike 단백질에 결합하는지만 보면 되기 때문에, 즉 분리된 단백질만 사용하는 실험이기 때문에 일반적인 실험실 환경 (위에 언급한 BSL2)에서 실험이 가능. 반면에 중화항체의 경우 살아있는 바이러스가 세포를 감염시키는지를 봐야하기 때문에 BSL4 환경에서 실험을 해야함. 물론 SARS-CoV-2의 Spike를 다른 바이러스로 옮긴 가짜 바이러스 (pseudovirus)를 사용할 수도 있겠으나 동물실험이 아닌 임상시험인 만큼 진짜배기 생바이러스 실험을 해야할 것으로 봄. 아래 언급할 CanSino의 경우 둘 다 했음. BSL4 실험실은 모더나 회사내에 있는지 없는지는 모르겠으나 미국 전역에 13군데 밖에 없다고 함. 아마도 BSL4가 있는 기관에 샘플을 보내서 실험을 해야할 것으로 보임. 요즘 BSL4 수요가 엄청 많을테니 분명 병목현상이 있을 듯.
부작용의 경우 25, 100ug 접종군에서는 접종 부위 홍반이 각각 한명씩, 250ug 군에서는 3명이 관찰됨. 임상 3상의 용량은 50, 100ug으로 결정됨. 임상 2상은 이달 내에, 임상 3상은 7월에 시작 예정.
이번주 모더나의 이번 임상 결과에 대해 왈가왈부 말이 많았는데… 이에 대한 개인적인 의견과 모더나의 밸류에이션에 대해서는 포스팅을 여러개 올렸으니 참고 바람.
▶Moderna Inc (MRNA) - 밸류에이션에 대해
▶Moderna Inc (MRNA) - 유상증자, 몬세프 슬라위
▶Moderna Inc (MRNA): STAT news
▶Moderna CEO가 언론 인터뷰로 주가 올리고 주식 팔았다???
CanSino Biologics (OTC:CASBF): 중국의 CanSino에서 개발중인 백신 후보물질 Ad5 vectored COVID-19 vaccine의 임상 1상 초기 결과를 의학 전문지 The Lancet에 발표. 18~60세 건강한 성인 108명을 대상으로 5 × 10^10, 1 × 10^11, 1.5 × 10^11 세가지 용량을 근육주사로 3/16~3/27 사이 한번 접종. 항체 생성은 14일차와 28일차에서 용량, 기간에 비례해서 나타났고 접종 전 대비 항체 생성 최소 4배 이상은 각 그룹당 28일차에 97% (35/36), 94% (35/36), 100% (36/36). 중화항체 최소 4배 이상 증가는 각 그룹당 50% (18/36), 50% (18/36), 75% (27/36)을 보임. 부작용은 광범위하게 (최소 한가지 이상 부작용 발생 81%) 나타났지만 용량에 비례해서 나타나지는 않음.
이번 발표는 모더나의 보도자료에 며칠 뒤지기는 했지만 COVID-19 백신의 임상사험에 대한 최초의 학술지 보고. 어찌보면 모더나 보도자료보다 훨신 의미있는 발표임에도 미국 언론에 이에 대한 기사는 많지 않음. 금요일 장중에 논문이 나왔는데 주식시장에 별다른 반응이 없었음. 요즘 중국과 핏대세우고 있어서 그런건지… 다음주에 있으려나? 근데 임상시험 결과에 대한 요약 보도자료가 나가고 한참 뒤에 학술지 발표가 나가는 일반적인 패턴과 달리, 모더나와는 반대로 CanSino 홈페이지에는 아예 데이타에 대한 보도자료는 커녕 논문을 냈다는 보도자료 조차 없음. 주주에게 어필해야하는 미국 상장 기업이 아니라서 그런건지.
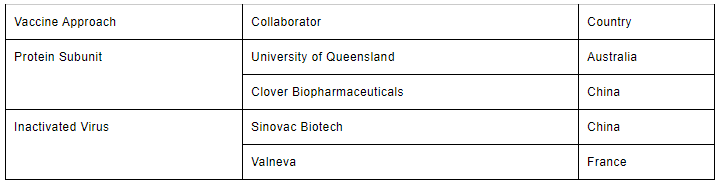
Dynavax Technologies Corp (DVAX): Dynavax가 애쥬반트 CpG 1018을 공급하는 협업사들 중 한두개가 7월까지 임상 1상을 시작한다고 발표. Dynavax의 CpG 1018을 사용하는 백신은 아래 표와 같음. 이중 2주전 Sinovac이 임상1상 준비중이라 발표했고 University of Queensland는 판데믹 초기 CEPI의 지원을 받은 4개의 프로젝트 중 하나라 이 둘이 아닐까 짐작해봄. 현재 애쥬반트 공급으로 다수의 협업계약을 맺고 있는 기업은 Dynavax와 GSK 두군데. 어찌보면 나중에 돈벌곳은 이 두군데가 아닐지. GSK는 뭐 거대기업이고...
※ 애쥬반트: 항원만으로는 부족할 수 있는 면역반응을 도와 항체 생성이 잘 일어나도록 면역을 증강시킬 목적으로 백신에 첨가되는 물질.
Kindred Biosciences (NASDAQ:KIN), Vaxart (NASDAQ:VXRT): Vaxart의 경구용 COVID-19 백신의 제조를Kindred Biosciences가 담당하기로 계약 체결.
Inovio Pharmaceuticals (NASDAQ:INO): 백신 후보물질 INO-4800의 동물실험 데이타를 Nature Communications에 발표. 쥐와 기니피그에서 결합 항체, 중화 항체를 만들었고 높은 수준의 T세포 반응을 보였음. ADE에 대한 언급은 없음.
IMV (NASDAQ:IMV): 펩타이드 epitope 후보군에서 23개의 펩타이드를 골라 DPX-COVID-19 백신 후보물질을 선정했다고 발표. 동물실험에서 강한 면역 반응을 보였음. 올 여름에 임상 1상 시작 예정. Epitope은 항원에서 실제 항체와 결합하게 되는 부위로 항체는 이 부위에 반응해서 만들어짐. 단백질의 경우 약 8~11개의 아미노산으로 구성된 펩타이드가 epitope 역할을 함.
| Symbol | Name | Weekly Gain | 시가총액($) |
| S&P500 | S&P 500 Index | 3.20% | |
| Nasdaq | Nasdaq Composite | 3.44% | |
| 바이오텍 (XBI) | SPDR S&P Biotech | 3.29% | |
| 바이오텍 (NBI) | NASDAQ Biotechnology Index | 1.00% | |
| IMV | Imv Inc | 53.48% | 296.8M |
| ATOS | Atossa Therapeutics Inc | 35.88% | 21.3M |
| NK | Nantkwest Inc | 27.98% | 549.7M |
| DVAX | Dynavax Technologies Corporation | 12.75% | 472.9M |
| VIR | Vir Biotechnology Inc | 11.00% | 4.0B |
| CASBF | Cansino Biologics Inc | 8.93% | 49.4B |
| ADMA | ADMA Biologics Inc | 8.40% | 245.2M |
| KIN | Kindred Biosciences Inc | 6.22% | 201.2M |
| INO | Inovio Pharmaceuticals Inc | 4.84% | 2.2B |
| VXRT | Vaxart Inc | 4.30% | 215.9M |
| MRNA | Moderna Inc | 3.46% | 26.8B |
| AZN | AstraZeneca plc | 3.39% | 72.5B |
| GOOGL | Alphabet Inc Class A | 2.93% | 963.4B |
| GOOG | Alphabet Inc Class C | 2.71% | 963.4B |
| ABT | Abbott Laboratories | 1.76% | 161.8B |
| CYDY | CytoDyn Inc | 1.64% | 1.5B |
| GSK | GlaxoSmithKline plc | -0.05% | 205.1B |
| TMO | Thermo Fisher Scientific Inc. | -0.78% | 134.4B |
| GENE | Genetic Technologies Limited | -1.64% | 23.1M |
| GILD | Gilead Sciences, Inc. | -3.83% | 92.0B |
| ALDX | Aldeyra Therapeutics Inc | -5.11% | 127.2M |
| AMRN | Amarin Corporation plc | -6.34% | 2.8B |
| BDX | Becton Dickinson and Co | -7.36% | 69.1B |
| FLGT | Fulgent Genetics Inc | -7.50% | 328.9M |
| OSUR | OraSure Technologies, Inc. | -9.22% | 922.9M |
| CEMI | Chembio Diagnostics Inc | -10.46% | 219.2M |
| QDEL | Quidel Corporation | -12.05% | 7.3B |
| NNVC | NanoViricides Inc | -21.39% | 56.2M |
| SRNE | Sorrento Therapeutics Inc | -25.00% | 1.0B |
▶1분기에 아마존보다 높은 매출 증가율을 보인 S&P500 기업들 (feat. Vertex Pharma)
'Covid-19' 카테고리의 다른 글
| Operation Warp Speed 다섯 백신 프로그램 선정 (0) | 2020.06.04 |
|---|---|
| Weekly COVID-19 Review 20200529 (0) | 2020.05.31 |
| Weekly COVID-19 Review 20200515 (0) | 2020.05.17 |
| Weekly COVID-19 Review 20200508 (0) | 2020.05.10 |
| Weekly COVID-19 Review 20200501 (0) | 2020.05.04 |
