코로나-19 백신 개발을 통해서 본 백신 플랫폼
백신이란?
항원, 즉 병원체를 약하게 만들어 인체에 주입하여 항체를 형성하게 하여 그 질병에 저항하는 후천 면역이 생기도록 하는 의약품 (출처:위키피디아)
WHO의 4/4자 자료를 보면 현재 SARS-CoV-2에 대한 백신은 총 62개가 개발중이고 그중 2개가 임상시험에 진입해 있습니다. 하나는 미국 주식하시는 분들에게 잘 알려진 Moderna (MRNA)의 mRNA 백신이고, 다른 하나는 중국 CanSino Biological Inc./Beijing Institute of Biotechnology가 개발중인 아데노바이러스 백신입니다. 두 백신 모두 현재 임상 1상을 진행중입니다.
작년 12월말에 WHO에 신종 폐렴질환이 보고되고, 곧이어 이 질병이 신종 코로나바이러스에 의한 질병이 밝혀지고 1월 10일 중국의 과학자들이 신종 코로나바이러스의 염기서열을 밝혀 낸 이후 각국의 여러 바이오텍/제약업체들과 아카데미 연구기관들이 백신 개발에 뛰어들었습니다. 위에서 언급한대로 현재 80여군데가 넘는 곳에서 SARS-CoV-2에 대한 백신을 개발중인데, 이 백신들 중에는 아직껏 승인받은 백신에 사용된적 없던 기술이 사용되는 것부터 전통적인 방식까지 여러가지 종류가 존재합니다.
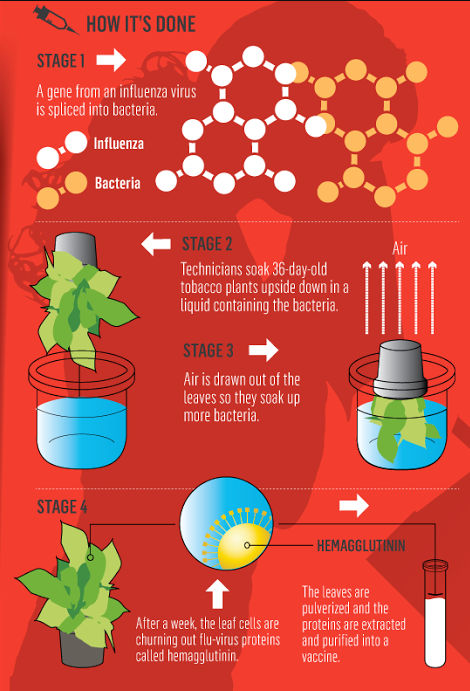
전통적인 백신의 생산 방식은 살아있는 바이러스나 박테리아를 계란 수정란에 주사해 감염시켜 증식시킨 후 이를 체내에서 증식하지 못하도록 비활성화 시킨 후 사람에게 사용하는 방식입니다. 최근에는 병원균을 세포 배양을 통해 증식시키거나, Britsh American Tobbaco, Philip Morris 등 담배회사의 백신개발 발표처럼 담뱃잎에서 증식시키는 방식도 사용하는 것 같습니다.
비활성화 시키는 방식은 크게 두가지로 수정란이나 세포에 여러차례 반복적으로 감염시켜 증식함으로써 사람에게 주사했을때 증식되는 능력을 없애는 방식 (live attenuated)와 화학처리를 해서 아예 불활성화 (inactivated) 시키는 방식이 있습니다. 살아있는 병원균을 증식시켜 백신을 만드는 방식은 병원균을 증식시키는데 오랜 기간이 걸리고, 비활성화가 잘 되지 않았을 때 바이러스가 체내에서 증식될 위험이 있다는 단점이 있는 반면, 바이러스 자체를 병원균으로 쓰기 때문에 바이러스의 여러부위에 결합하는 항체가 생성될 수 있어서 변종이 발생할 경우에도 항체결합부위 전부가 변종되지 않는 이상 바이러스를 막는 효과를 낼 수가 있습니다.
이처럼 병원균을 살아있는채로 증식시키는 방식이 있는가하면, 바이러스의 껍데기에서 항체와 반응할만한 부위를 찾아서 그 단백질만을 생산해 백신으로 만드는 방식이 있습니다. 아래 SARS-CoV-2의 그림에서 노란색으로 표시된 돌출부위가 Spike라는 단백질입니다. 바이러스의 표면에 돌출되어 있는 만큼 항체와 반응하기가 쉽고, 그래서 이 단백질을 항원으로 사용해서 만드는 백신이 대다수입니다.

이러한 재조합 단백질 방식은 항원으로 사용할 단백질을 정제해서 사용하는 방식과 항원으로 사용할 단백질을 암호화하고 있는 mRNA나 DNA등 핵산을 이용하는 방식으로 크게 나눌 수 있습니다. 단백질 정제 방식은 다시 재조합 단백질을 생합성하는 방식과 단백질 내 항원 펩타이드를 합성하는 방식, Virus-like particles (VLP)를 사용하는 방식으로 나눌 수 있습니다.
핵산 방식은 다시 RNA 방식과 DNA 방식으로 나눌 수 있습니다. 핵산은 몸안에 들어가도 그 자체로는 항원 역할을 할 수가 없고 세포에 들어가서 세포내 단백질 합성 기제를 이용해서 항원 단백질을 만들어내야 합니다. 그래서 DNA와 RNA를 세포에 전달하는 방식에 따라 다시 구분되어집니다. RNA의 경우 나노지질입자 (Lipid Nano Particle, LNP)에 실어 전달하는 방식만 있으나 DNA의 경우 복제 불가능한 바이러스 벡터에 싣는 방식 (Non Replicating Viral Vector), 복제 가능한 바이러스 벡터에 싣는 방식 (Replicating Viral Vector), 나노지질입자 (Lipid Nano Particle, LNP)에 싣는 방식, 벡터 없이 DNA만 전기화학적인 방법으로 전달하는 방식 등으로 나눌 수 있습니다. 여기서 벡터 역할을 하는 바이러스는 병원균인 바이러스가 아니고 사람 인체에 들어가도 안전한 바이러스를 이용합니다.
재조합 단백질 백신은 바이러스 전체를 항원으로 사용하는 백신에 비해 더 강한 면역반응을 일으킬 수 있다는 장점이 있습니다. 하지만 단백질 생산에 비교적 오랜 시간이 걸리고 비용도 많이 들기 때문에 최근에는 DNA/RNA 백신이 새로운 대안으로 떠오르고 있습니다. DNA/RNA 백신은 단백질을 암호화한 유전자를 투여하는 방식이기 때문에 단백질 생합성 및 분리에 드는 시간과 비용을 줄일 수 있고, 벡터를 사용하지 않는 DNA, RNA 백신의 경우 생합성이 아닌 화학합성을 하기 때문에 시간을 더욱 단축할 수 있습니다. Moderna의 mRNA 백신이 SARS-CoV-2의 유전자 염기서열이 밝혀진 후 불과 한달여만에 후보물질을 만들어낼 수 있었던 이유입니다.
하지만 단점은 바이러스의 유전자 변이입니다. 접종하는 항원의 갯수에 제한이 있다보니 변종이 생겨 백신에 사용된 항원과 달라지는 경우 새로운 백신을 만들어야한다는 단점이 있습니다. 물론 단백질 하나에서 여러 부위가 항원으로 사용되기 때문에 한두 군데의 변종에는 여전히 적용 가능하지만, 바이러스 전체를 백신으로 사용하는 경우 바이러스의 수많은 부위에 대해 항체가 만들어지기 때문에 비교적 변종에 대응할 수가 있습니다. 반면 빠른 개발이 용이하기 때문에 변종 발생시 변종에 대한 백신 개발도 빨리 이루어질 수 있기도 합니다.

아래 표는 WHO에서 정리한 현재 개발중인 62개의 백신에 대해 제가 조금 살을 붙인겁니다. 미국에 상장되어 있는 기업들의 경우 심볼이 추가되었고, 외부 펀딩 (CEPI, BARDA 등)을 받아 개발중인 백신도 따로 표기했습니다. 백신 개발에 있어 외부 펀딩은 매우 중요합니다. 인플루엔자 처럼 매년 찾아오는 유행병인 경우도 있지만 SARS, MERS, ZIKA 처럼 한두해 반짝 왔다가 사라져 버리는 경우도 많이 있었습니다. SARS나 ZIKA의 경우 아직도 백신이 없는데, 그 이유가 질병의 유행이 끝나면서 백신개발 프로젝트에 대한 정부 지원이 끊겨버리는 바람에 백신을 개발하던 기업들이 아무도 사지 않을 백신을 자비를 들여 끝까지 개발할 동력을 상실해버렸기 때문입니다. 현재 수많은 기업, 연구기관들이 코로나-19 백신 개발에 뛰어들었지만 발빠르게 움직인 기업들은 대부분 소형 바이오텍들이었고, 대형 제약사들은 뒤에 천천히 들어왔습니다. 끝까지 개발할 만한 가치가 있는지 아마도 계산기 돌리는 시간이 필요했던 것 같습니다. 빅파마를 제외하고 임상 2/3상까지 펀딩을 마련해 놓은 기업은 1상은 CEPI, 2/3상은 BARDA의 지원을 받는 Moderna가 현재로서는 유일합니다. 현재 백신개발 프로젝트를 진행하고 있는 대사수의 나노캡 바이오텍들은 외부 펀딩 없이 시작했고, 백신 개발을 끝까지 지속하지 못할 가능성이 높습니다.
| Platform | Type of candidate vaccine | Developer | Symbol (USA) | Current stage of clinical evaluation/regulatory status- Coronavirus candidate | Same platform for non-Coronavirus candidates | External Funding |
| Live Attenuated Virus | Deoptimized live attenuated vaccines | Codagenix/Serum Institute of India | Pre-Clinical | HAV, InfA, ZIKV, FMD, SIV, RSV, DENV | ||
| Live Attenuated Virus | Measles Virus (S, N targets) | DZIF – German Center for Infection Research | Pre-clinical | Zika, H7N9, CHIKV | ||
| Inactivated | Inactivated + alum | Sinovac | Pre-Clinical | SARS | ||
| Inactivated | Inactivated | Beijing Institute of Biological Products/Wuhan Institute of Biological Products | Pre-Clinical | |||
| Inactivated | TBD | Osaka University/ BIKEN/ NIBIOHN | Pre-Clinical | |||
| Protein Subunit | Capsid-like Particle | AdaptVac (PREVENT-nCoV consortium) | Pre-Clinical | |||
| Protein Subunit | Drosophila S2 insect cell expression system VLPs | ExpreS2ion | Pre-Clinical | |||
| Protein Subunit | S protein | WRAIR/USAMRIID | Pre-Clinical | |||
| Protein Subunit | S protein + Adjuvant | National Institute of Infectious Disease, Japan | Pre-Clinical | Influenza | ||
| Protein Subunit | VLP recombinant protein + Adjuvant | Osaka University/ BIKEN/ National Institutes of Biomedical Innovation, Japan | Pre-Clinical | |||
| Protein Subunit | Native like Trimeric subunit Spike Protein vaccine | Clover Biopharmaceuticals Inc./GSK/Dynavax | GSK/DVAX | Pre-Clinical | HIV, REV Influenza | |
| Protein Subunit | microneedle arrays S1 subunit | Univ. of Pittsburgh | Pre-Clinical | MERS | ||
| Protein Subunit | Peptide | Vaxil Bio | Pre-Clinical | |||
| Protein Subunit | Adjuvanted protein subunit (RBD) | Biological E Ltd | Pre-Clinical | |||
| Protein Subunit | Peptide | Flow Pharma Inc | Pre-Clinical | Ebola, Marburg, HIV, Zika, Influenza, HPV therapeutic vaccine, BreastCA vaccine | ||
| Protein Subunit | S protein | AJ Vaccines | Pre-Clinical | |||
| Protein Subunit | Ii-Key peptide | Generex/EpiVax | GNBT | Pre-Clinical | Influenza, HIV, SARS-CoV | |
| Protein Subunit | S protein | EpiVax/Univ. of Georgia | Pre-Clinical | H7N9 | ||
| Protein Subunit | S protein (baculovirus production) | Sanofi Pasteur | SNY | Pre-Clinical | Influenza, SARS-CoV | BARDA |
| Protein Subunit | VLP recombinant protein nanoparticle vaccine + Matrix M | Novavax | NVAX | Pre-Clinical | RSV; CCHF, HPV, VZV, EBOV | CEPI |
| Protein Subunit | gp-96 backbone | Heat Biologics/Univ. Of Miami | HTBX | Pre-Clinical | NSCLC, HIV, malaria, Zika | |
| Protein Subunit | Molecular clamp stabilized Spike protein | University of Queensland/GSK/Dynavax | GSK/DVAX | Pre-Clinical | Nipah, influenza, Ebola, Lassa | CEPI |
| Protein Subunit | S1 or RBD protein | Baylor College of Medicine | Pre-Clinical | SARS | ||
| Protein Subunit | Subunit protein, plant produced | iBio/CC-Pharming | IBIO | Pre-Clinical | ||
| Protein Subunit | Recombinant protein, nanoparticles (based on S protein and other epitopes) |
Saint-Petersburg scientific research institute of vaccines and serums | Pre-Clinical | |||
| Protein Subunit | COVID-19 XWG-03 truncated S (spike) proteins | Innovax/Xiamen Univ./GSK | GSK | Pre-Clinical | HPV | |
| Protein Subunit | Adjuvanted microsphere peptide | VIDO-InterVac, University of Saskatchewan | Pre-Clinical | |||
| Protein Subunit | Synthetic Long Peptide Vaccine candidate for S and M proteins | OncoGen | Pre-Clinical | |||
| VLP | Plant-derived VLP | Medicago Inc. | Pre-Clinical | Flu, Rotavirus, Norovirus, West Nile virus, Cancer | ||
| VLP | ADDomerTM multiepitope display | Imophoron Ltd and Bristol University’s Max Planck Centre | Pre-Clinical | |||
| Non Replicating Viral Vector | Adenovirus Type 5 Vector | CanSino Biological Inc./Beijing Institute of Biotechnology | Phase 1 ChiCTR2000030906 | Ebola | ||
| Non Replicating Viral Vector | ChAdOx1 | University of Oxford | Phase 1/2 (not yet recruiting) NCT04324606 | MERS, influenza, TB, Chikungunya, Zika, MenB, plague | CEPI | |
| Non Replicating Viral Vector | MVA encoded VLP | GeoVax/BravoVax | Pre-Clinical | LASV, EBOV, MARV, HIV | ||
| Non Replicating Viral Vector | Ad26 (alone or with MVA boost) | Janssen Pharmaceutical Companies | JNJ | Pre-Clinical | Ebola, HIV, RSV | BARDA |
| Non Replicating Viral Vector | MVA-S encoded | DZIF – German Center for Infection Research | Pre-clinical | Many | ||
| Non Replicating Viral Vector | adenovirus based NasoVAX expressing SARS2-CoV spike protein | Altimmune | ALT | Pre-Clinical | influenza | |
| Non Replicating Viral Vector | Ad5 S (GREVAX™ platform) | Greffex | Pre-Clinical | MERS | ||
| Non Replicating Viral Vector | Oral Vaccine platform | Vaxart | VXRT | Pre-Clinical | InfA, CHIKV, LASV, NORV; EBOV, RVF, HBV, VEE | |
| Replicating Viral Vector | Measles Vector | Zydus Cadila | Pre-Clinical | |||
| Replicating Viral Vector | Measles Vector | Institute Pasteur/Themis/Univ. of Pittsburg Center for Vaccine Research | Pre-Clinical | West nile, chik, Ebola, Lassa, Zika | ||
| Replicating Viral Vector | Horsepox vector expressing S protein | Tonix Pharma/Southern Research | TNXP | Pre-Clinical | Smallpox, monkeypox | |
| Replicating Viral Vector | Influenza vector expressing RBD | University of Hong Kong | Pre-Clinical | |||
| Replicating Viral Vector | VSV vector expressing S protein | IAVI/Batavia | Pre-Clinical | Ebola, Marburg, Lassa | ||
| DNA | DNA plasmid vaccine Electroporation device | Inovio Pharmaceuticals | INO | Pre-Clinical | Lassa, Nipah, HIV, Filovirus, HPV, Cancer indications, Zika, Hepatitis B | CEPI |
| DNA | DNA with electroporation | Karolinska Institute / Cobra Biologics (OPENCORONA Project) | Pre-Clinical | |||
| DNA | DNA plasmid vaccine | Osaka University/ AnGes/ Takara Bio | Pre-Clinical | |||
| DNA | DNA | Takis/Applied DNA Sciences/Evvivax | Pre-Clinical | |||
| DNA | DNA plasmid vaccine | Zydus Cadila | Pre-Clinical | |||
| RNA | LNP encapsulated mRNA | Moderna/NIAID | MRNA | Phase 1 NCT04283461 | multiple candidates | CEPI, BARDA |
| RNA | LNP encapsulated mRNA cocktail encoding VLP | Fudan University/ Shanghai JiaoTong University/RNACure Biopharma | Pre-Clinical | |||
| RNA | LNP encapsulated mRNA encoding RBD | Fudan University/ Shanghai JiaoTong University/RNACure Biopharma | Pre-Clinical | |||
| RNA | LNP encapsulated mRNA | University of Tokyo/ Daiichi-Sankyo | Pre-Clinical | MERS | ||
| RNA | mRNA | China CDC/Tongji University/Stermina | Pre-Clinical | |||
| RNA | mRNA | Arcturus/Duke-NUS | ARCT | Pre-Clinical | multiple candidates | |
| RNA | mRNA | BioNTech/Fosun Pharma/Pfizer | BNTX, PFE | Pre-Clinical | ||
| RNA | mRNA | Curevac | Pre-Clinical | RABV, LASV, YFV; MERS, InfA, ZIKV, DengV, NIPV | CEPI | |
| RNA | saRNA | Imperial College London | Pre-Clinical | EBOV; LASV, MARV, Inf (H7N9), RABV | ||
| Unknown | Unknown | ReiThera | Pre-Clinical | |||
| Unknown | Unknown | BioNet Asia | Pre-Clinical | |||
| Unknown | Unknown | ImmunoPrecise | Pre-Clinical | |||
| Unknown | Unknown | MIGAL Galilee Research Institute | Pre-Clinical | |||
| Unknown | Unknown | Doherty Institute | Pre-Clinical | |||
| Unknown | Unknown | Tulane University | Pre-Clinical |
'Covid-19' 카테고리의 다른 글
| Weekly COVID-19 Review 20200417 (4) | 2020.04.18 |
|---|---|
| Weekly COVID-19 Review 20200410 (2) | 2020.04.11 |
| Furlough 3/29~4/4, 몇가지 트랜드 (2) | 2020.04.05 |
| Weekly COVID-19 Review 20200403 (24) | 2020.04.04 |
| FDA 승인 RNA 진단법 민감도 비교 (4) | 2020.04.02 |
