위기인가 기회인가? 유전자 치료제 선두 기업 bluebird bio
작성일 2021.3.6
#bluebird bio (BLUE) #Bristol-Myers Squibb (BMY) #CRISPR Therapeutics (CRSP) #Vertex Pharmaceuticals (VRTX) #Johnson & Johnson (JNJ) #Legend Biotech (LEGN) #Regeneron Pharmaceuticals (REGN) #Novo Nordisk (NVO)
-------------------------------------------------<Key Point>--------------------------------------------
❏ 초기 유전자 치료제 개발 기업인 불루버드 바이오는 뛰어난 효능을 보이며 상용화가 임박한 유전자 치료제와 CAR-T 후보물질들을 보유하고 있다. 2017-2018년 CAR-T 기업 인수합병 붐을 타고 글로벌 빅파마들의 인수합병 1순위로 거론되면서 주가도 고공행진했었다.
❏ 그러나 잇따른 악재로 주가가 3년여간 하락 추세에 있으며 최근에는 임상시험 참가자에게서 암이 발병하면서 최대의 위기를 맞았다.
❏ 지난 3년간 시가총액이 1/5 이하로 쪼그라들면서 2013년 상장 당시 주가로 돌아간 불루버드 바이오는 과연 투자자들에게 새로운 기회를 선사하며 기사회생할 수 있을까?
-------------------------------------------------<본 내용>-------------------------------------------------
잇따른 악재, 그리고 백혈병까지, 위기의 불루버드 바이오
2020년 바이오 업종은 나스닥 바이오텍 지수 31%, 대표적인 바이오테크 ETF XBI 56%가 상승하며 16% 상승한 S&P 500, 44% 상승한 나스닥을 아웃퍼폼했다. 하지만 바이오 업종 내에서 상승에 동참하지 못했던 분야가 있는데 유전자 치료제 분야다. 2019년 총 6건의 유전자 치료제 기업 인수합병 발표로 2020년 초반까지 상승 무드를 이어가던 유전자 치료제 분야는 2020년 들어 다수의 부작용 발생 및 임상시험 중단 권고, 까다로워진 규제 당국의 요구 조건 등 분야 전반의 악재가 잇따르면서 침체에 들어갔다.
유전자 치료제 기업들 가운데 특별히 더 하락세가 심했던 기업은 유전자 치료제 분야의 선도 기업이자 초기 CAR-T 개발 기업들 가운데 하나인 불루버드 바이오다. 유전자 치료제를 개발중인 기업들 가운데 가장 앞선 파이프라인들을 보유한 기업이기도한 불루버드 바이오는 2017~2018년 Gilead Siences의 Kite Pharma 인수 ($11.9B), Celgene의 Juno Therapeutics 인수 ($9B) 등 초기 CAR-T 개발 기업 대형 인수합병 붐을 타고 한때 인수합병 1순위로 거론되며 뜨거운 관심을 모았었다.
그러나 2018년 3월 주가 $206, 시가총액 $11.7B으로 사상 최고치를 기록한 이후 반복적인 임상시험 결과 발표 지연, FDA 승인 신청 지연, 서류 미비 및 제조 공정 이슈로 인한 FDA의 추가 서류 요청, 강력한 경쟁자의 등장 등의 악재가 잇따랐고 주가는 3년간 하향 추세가 지속되며 $40대까지 하락했다.
그리고 올해 2월 16일 불루버드 바이오의 주가 하락세에 화룡 정점을 찍는 사건이 발생했다.
겸상 적혈구증에 대한 임상시험에 참여해 5년전 유전자 치료제 투여를 받은 두명의 환자에게서 한 명은 백혈병이, 다른 한 명은 골수 형성 이상 증후군이 발생한 것이다. 백혈병은 불루버드가 유전자의 전달체로 사용하는 렌티바이러스/레트로바이러스 계열의 백터를 사용한 경우 이전에도 보고가 있던 부작용이다.
불루버드 바이오는 동일한 렌티바이러스 벡터를 이용한 유전자 치료 임상시험 및 상용화된 ZYNTEGLO의 판매를 잠정 중단했다. 주가는 2013년 상장일 가격보다 낮은 $24대까지 폭락했다. 그러나 일주일 후 CEO가 한 투자자 미팅에서 잠정 조사 결과 백혈병 발생은 유전자 치료와 무관하고 골수 형성 이상 증후군은 오진일 가능성을 언급하며 주가는 일단 하락세를 멈췄다.
불루버드 바이오에 대해 알아보기 전에 이번 폭락을 야기한 유전자 치료제의 전달체인 벡터에 대해 살펴보자.
유전자 치료 벡터
유전자 치료는 광범위하게는 유전자 편집, RNAi, 안티센스 RNA, mRNA 치료 등을 포함하지만 통상적으로는 유전자를 DNA 형태로 전달체인 벡터에 실어 세포에 전달하는 일회성 치료를 의미한다. 주로 하나의 유전자에 돌연변이가 발생해서 유발된 질병 (monogenic diseases)에 정상 유전자 혹은 돌연변이 유전자의 정상 기능을 회복시켜주는 유전자를 단 한차례의 투여로 영구적인 혹은 장기간의 치료효과를 보는 것을 목적으로 한다.
유전자 치료를 DNA 형태로 전달하는 이유는 RNA나 단백질 투여는 반복 투여가 필요한 반면, DNA 형태로 전달하면 전달체인 벡터에 따라 일회 투여만으로 반영구적으로 세포에 존재하며 치료 효과를 보이는 것이 가능하기 때문이다.
전달체로 사용되는 벡터는 크게 바이러스 벡터와 비 바이러스 벡터로 분류된다. 바이러스 벡터는 바이러스가 사람 세포에 침투해 숙주 세포를 통해 자신의 단백질을 만드는 성질을 이용하는 방식이다. 비 바이러스 벡터는 DNA를 직접 주입하거나 지질 나노 입자 등에 실어 전달하는 방식으로 바이러스 벡터에 비해 많은 장점이 있으나 아직은 세포 전달, 단백질 발현 효율에서 바이러스 방식만큼의 효과를 보지 못해 바이러스 벡터 방식이 더 널리 이용되고 있다.
바이러스 벡터는 초기에는 아데노바이러스, 레트로바이러스가 주로 사용됐으나 현재는 아데노연관바이러스(AAV)와 렌티바이러스가 주로 사용된다. 바이러스 벡터들 간의 가장 큰 차이점은 세포에 들어갔을 때 염색체에 삽입되는지 여부다. 아데노바이러스와 AAV는 세포에 침투한 후 바이러스 DNA가 숙주 세포 염색체에 삽입되지 않고 독립적으로 핵에 존재한다. 반면 레트로바이러스와 렌티바이러스의 DNA는 숙주세포의 염색체에 삽입된다.
바이러스 유전자가 숙주세포 염색체에 삽입될 때에는 삽입 부위가 무작위로 정해지기 때문에 자칫 중요한 유전자에 영구적인 손상이 일어날 수 있다. 가령 바이러스 유전자 삽입으로 암 억제 유전자가 망가지거나, 반대로 암 유발 유전자가 활성화되는 경우 암이 발생할 수 있고 실제로 과거 레트로바이러스를 이용한 유전자 치료에서 백혈병 발생이 보고된 바 있다.
따라서 최근에는 AAV를 주로 벡터로 사용하고 있지만 골수 세포 등 세포분열이 왕성하게 일어나는 세포를 타게팅하는 경우에는 레트로바이러스나 렌티바이러스를 사용할 수밖에 없다. AAV의 경우 염색체에 삽입되지 않아서 세포 분열이 일어나면서 소실되기 때문이다.
렌티바이러스 벡터 유전자 치료의 선도 기업 불루버드 바이오
불루버드 바이오는 두명의 MIT 교수들이 1992년에 설립한 초기 유전자 치료제 기업들 가운데 하나로 매사츄세츠주 캠브릿지에 소재해 있다. 2013년 나스닥에 상장했다. 렌티바이러스를 벡터로 사용한 유전자 및 세포 치료제를 개발하는 기업으로 이 분야 선두 기업이다.
중중 유전성 질환에 대한 유전자 치료제와 유전자 조작된 면역세포를 이용한 항암 세포치료제 CAR-T를 개발하고 있으며 상용화된 제품은 2019년 EU에서 겸상적혈구증에 대해 승인받은 ZYNTEGLO가 있다. 올해 말 항암제 파이프라인을 분리해 신규 기업으로 스핀오프할 계획을 가지고 있다.
| 기준일자 | 2021.3.6 | 52주 최저-최고가 | $24.24 - $72.51 |
| 기업명 (심볼) | bluebird bio, Inc(BLUE) | 90일 평균 거래량 | 2,052,521 |
| 업종 | 헬스케어 | P/E (TTM) | N/A |
| 시가총액 | $1.926 | EPS (TTM) | -$9.95 |
| 현재주가 | $28.68 | 배당금 | 없음 |
파이프라인 및 포트폴리오
불루버드 바이오의 파이프라인은 크게 중증 유전 질환과 항암제로 나뉜다. 불루버드 바이오의 치료제 후보들은 모두 렌티바이러스 벡터를 유전자 전달체로 사용한다는 점 이외에 ex vivo 방식의 유전자 치료라는 공통점이 있다. ex vivo 방식에 대해서는 필자의 <2021년 주목해야할 바이오 키워드 ‘유전자 편집’> 편을 참고하기 바란다.
1. 중증 유전 질환
중증 유전 질환 치료제 후보물질은 beti-cel (LentiGlobin)과 eli-cel 두 종류를 개발 중이다. 두 후보물질 모두 환자 본인의 조혈 모세포를 채취해서 돌연변이가 발생한 발병 유전자의 정상 카피를 렌티바이러스 벡터에 실어 세포에 주입한 후 정맥주사를 통해 다시 체내로 되돌려 보내는 치료법이다.
1.1. beti-cel (Betibeglogene autotemcel, LentiGlobin)
수혈 의존적 베타 지중해 빈혈 (transfusion-depedent β-thalassemia, TDT)과 겸상적혈구증 (sickle cell disease, SCD) 두 적응증에 대해 개발하고 있다. 두 질병 모두 헤모글로빈을 형성하는 베타 글로빈 유전자에 돌연변이가 발생해서 생기는 질병이다.
1.1.1. 수혈 의존적 베타 지중해 빈혈 (TDT): TDT는 베타 글로빈 유전자의 돌연변이로 인해 결함이 있는 적혈구가 생성되는 질병이다. 빈혈, 비장 비대증, 골수 확장, 골격 기형 및 주요 기관의 철 과다가 발생하며 유전형에 따라 심한 경우 수혈을 필요로 한다. beti-cel은 정상 베타 글로빈 유전자를 지닌 조혈 모세포를 공급해 정상적인 적혈구가 생성되도록 하는 치료법이다. 2020년 12월 미국 혈액학 학회에서 beti-cel을 투여받은 환자가 최대 6년째 수혈없이 생활 가능하다는 것을 발표한 바 있다.
beti-cel은 2019년 6월 유럽에서 ZYNTEGLO 라는 브랜드명으로 β0/β0 유전형이 아닌 12세 이상의 TDT에 대해 승인을 받았다. ZYNTEGLO의 가격을 $1.8M (€1.58M)라는 고가에 책정하면서 승인은 받았지만 각 국가들과 지난한 보험 수가 협상을 벌였다. 유럽의 경우 승인은 EU 단위에서 하지만 보험 수가는 개별 국가별로 따로 협상해야한다. 불루버드는 가치 기반 지불 모델 도입. 20%만 선수금으로 받고 나머지 80%는 5년간 매년 치료 효과가 유지되는 경우에만 마일스톤으로 균등 지불받는 방식을 도입하며 협상을 별였지만 코로나-19가 겹치면서 첫 환자의 투여가 올해 2월에서야 독일에서 이뤄졌다. ZYNTEGLO의 판매는 암 환자 발생 이후 잠정 중단된 상태다.
블루버드는 올해 중반 (아마도 6월의 유럽 혈액학 학회 EHA가 유력)에 데이터 업데이트를 예고하고 있으며 암 환자 문제 해결을 전제로 2019년 4분기에 TDT의 모든 연령, 모든 유전형에 대해 시작한 FDA의 롤링 서류 제출 (rolling submission – 신속 승인 등 지정을 받은 후보물질들에 한해 승인 심사 서류를 일괄 제출하는 대신 각 섹터가 완성되는 대로 그때 그때 제출하는 제도)을 올해 중반 완료할 계획이다. 유럽에도 역시 연령대와 유전형을 확장한 승인 신청서를 제출할 예정이다.
1.1.2. 겸상 적혈구증 (sickle cell disease, SCD): SCD 역시 헤모글로빈을 형성하는 베타 글로빈 유전자에 돌연변이가 발생해 인해 적혈구가 낫 모양으로 형성되는 유전 질환이다. 낫 모양의 적혈구는 쉽게 파괴되서 빈혈을 일으키고 작은 혈관을 통과하지 못하고 혈관을 막아 혈류장애를 일으킨다. 혈류 장애를 일으킬 때 급성 통증을 동반하는데 이를 혈관막힘위기 (vaso-occlusive crises, VOC)라고 하며 이로 인해 일상 생활에 지장을 일으킨다.
불루버드는 TDT와 마찬가지로 beti-cel을 SCD의 유전자 치료제로 개발하고 있다. 현재 임상 3상 HGB-210을 진행중이며 2020년 12월 미국 혈액학 학회에서 임상 ½상 C 그룹 결과에서 beti-cel을 투여받은 환자가 6~24개월간 VOC 발생이 전무했다는 결과를 발표한 바 있다. 임상 ½상 장기 추적 결과 및 임상 3상 결과 업데이트도 올해 말 예고되어 있으며 임상 ½상 HGB-206 C 그룹 결과를 바탕으로 FDA와 신속 승인 신청에 합의가 되어 있다. FDA가 제조 공정상 추가 데이터를 요구했기 때문에 승인 신청은 2022년 말로 계획되어 있었는데 백혈병 문제가 발생했다. 하지만 안전성 문제만 해결된다면 예정된 시간에 신속 승인 신청이 가능할 것으로 보인다.
1.2. eli-cel (Elivaldogene autotemcel, Lenti-D)
불루버드는 eli-cel을 부산백질이영양증 소아대뇌형(cerebral adrenoleukodystrophy, CALD)에 대해 개발중이다. CALD는 ABCD1 유전자의 돌연변이로 인해 매우 긴사슬 지방산이 축적되어 발생하는 X-염색체 연관 희귀 대사 질환으로 부산백질이영양증 가운데 가장 심각한 형태다. CALD 환자는 뇌기능 상실로 인한 사고, 운동 장애가 발생하며 빠르게 진행되기 때문에 제때에 치료를 받지 못하면 사망한다.
eli-cel 역시 beti-cel과 마찬가지로 정상 ABCD1 유전자를 렌티바이러스 벡터를 통해 환자 본인의 조혈 모세포에 주입한 후 이 세포를 다시 환자에게 돌려보내는 ex-vivo 치료법이다.
2020년 8월 EBMT 학회에서 eli-cel을 투여받은 환자 87%가 24개월 이상 기능 장애 없이 생존해 있다는 임상 2/3상 Starbeam의 장기 추적 결과를 발표했다. 2020년 10월 유럽에서 승인 심사가 시작됐고 올해 중반 심사 결과 발표가 예상된다. 또한 FDA에 올해 중반 승인 신청서를 제출할 계획이다.
중증 유전 질환 파이프라인

출처: 불루버드 홈페이지. 2021.3.6. https://www.bluebirdbio.com/our-science/pipeline
2. 항암제
올해말 분사가 예정되어 있는 항암제 분야에서는 암세포를 공격하도록 유전자 조작한 여러 종류의 면역세포 치료제를 개발중이다. 가장 선두에 있는 후보물질은 다발성 골수종에 대해 개발중인 ide-cel (bb2121)이며, 이를 제외하면 모두 초기 단계에 있거나 전임상 단계에 있다.
2.1. ide-cel (bb2121)
ide-cel은 다발성 골수종의 표지 단백질인 BCMA를 인식하는 항체-T세포 수용체를 지닌 T세포 (chimeric antigen receptor T, CAR-T) 치료제다. CAR-T는 환자 본인의 혈액에서 T세포를 분리하고 암의 표지 단백질을 인식하는 항체-T세포 수용체 카이메라(항원 인식 부위는 항체를, 세포내 신호 전달 부위는 T세포 수용체를 지닌 혼합 단백질)를 바이러스 벡터를 통해 T세포에 주입한 후 시험관 배양을 거쳐 환자에게 되돌려 보내는 치료법이다. 환자 몸으로 되돌아간 CAR-T 세포는 BCMA 표지가 있는 암세포만을 공격하게 된다. CAR-T는 현존하는 항암 치료법 가운데 가장 뛰어난 효능을 보이지만 제조가 까다롭고 고가이며 과다 면역으로 인한 부작용이 심하다는 단점이 있다.
불루버드는 ide-cel을 브리스톨-마이어 스큅(BMS)과 공동으로 개발하고 있다. 임상 2상 KarMMa에서 최소한 3차례 이상의 치료법을 사용해도 치료가 되지 않는 치료법이 소진된 환자들을 대상으로 객관적 반응율 73%, 완전 관해 33%라는 놀라운 효능을 보였다. 최고 투여량에서는 객관적 반응율과 완전 관해 각각 94%, 42%를 보였다. 2020년 발표한 CRB-401 임상시험 역시 유사한 결과 (객관적 반응율, 완전 관해 각각 76%, 39%)를 보였다. 이 결과를 바탕으로 현재 FDA에서 우선 심사중이고 승인 심사일은 3월 27일이다. ide-cel은 승인시 BCMA를 타게팅하는 CAR-T로는 최초이며 블록버스터 후보로 꼽히고 있다. 불루버드는 ide-cel의 후속 후보물질 bb21217도 개발중이며 역시 BMS와 공동 개발하고 있다.
불루버드는 CAR-T 외에도 TCR-T, CCR-T, DARIC 등 다양한 형태의 항암 세포 치료제를 초기 및 전임상 단계에서 개발중이다. 또한 megaTAL이라는 유전자 편집 플랫폼도 개발중이다.
항암제 파이프라인
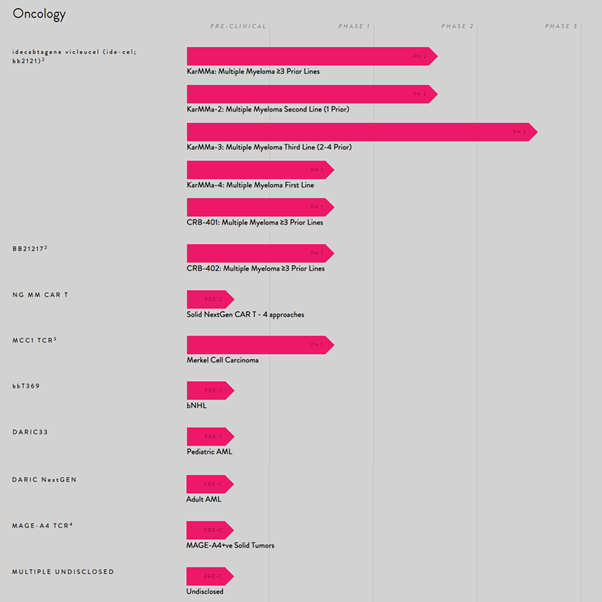
출처: 불루버드 홈페이지. 2021.3.6. https://www.bluebirdbio.com/our-science/pipeline
3. 협업 관계
불루버드는 BCMA CAR-T 개발을 오랜 기간 BMS에 인수된 셀진과 함께 해왔고 현재 상용화 문턱에 와있다. 이밖에 리제너론 파마슈티컬즈와 고형암에 대한 T세포 치료제 (MAGE-A4 TCR)개발을, 노보 노디스크와 혈우병에 대한 in vivo 유전자 편집 치료제를 개발중이다.
투자 의견
불루버드 바이오에 대한 투자 포인트를 간략히 정리해보면 다음과 같다.
1. 2023년까지 계속될 카탈리스트: beti-cel에서 발생한 백혈병 발생 이슈가 긍정적으로 마무리된다는 가정하에 약 3주 뒤인 3월 27일 FDA의 ide-cel 승인 심사를 시작으로 향후 2년간 현재 진행중인 후기 임상 3상 프로그램 네가지의 미국과 유럽에서의 승인 과정이 예고되어 있다. 네 프로그램 모두가 각 분야에서 first-in-class이고 상용화 된다면 선점자 우위(first-mover advantage)를 지닐 수 있다.
2. 저렴한 주가: 불루버드의 시가 총액은 약 $2B이다. 불루버드의 2020년 4분기말 기준 현금, 현금성 자산 및 유가증권 보유량은 약 $1.15B이며 부채는 없다. 기업가치 (enterprise value, EV, 시가총액 + 부채 – 현금성 자산 보유량. 기업 인수합병시 인수하는 기업이 실제 지불하는 비용)가 $1B도 되지 않는다는 뜻이다. 반면 Evaluate Pharma에서 추정하는 beti-cel의 2026년 SCD, TDT 적응증 예상 매출은 각각 $874M, $626M, ide-cel은 $1,425M이다. 매출 추정치가 나와있지 않은 eli-cel을 제외해도 예상 잠재 매출은 약 $2.9B에 달한다. 플랫폼 가치 역시 포함되지 않았다. 잠재 매출에 비해 현재의 기업 가치는 터무니없이 저렴하다.
3. 분사: 불루버드는 올해말 유전질환과 항암제 파트를 분사할 계획을 가지고 있다. 아직 구체적인 계획은 발표되지 않았지만 주주들에게 비과세로 신규 기업 지분이 돌아가고 현금 보유량도 적절히 분할한다고 한다. 유전질환의 경우 파이프라인 대부분이 상용화를 앞두고 있어서 상용화에 주력하는 기업이 될 전망이고, 항암제의 경우 BMS가 ide-cel 상용화를 담당하면서 파이프라인 개발에 집중하는 전략이다. 서로 다른 분야의 파이프라인들인 만큼 분사 후 더욱 효율적인 기업이 될 수 있다.
반면 리스크 요인은 다음과 같다.
1. 렌티바이러스 벡터: beti-cel 투여 환자에게서 발생한 두건의 부작용 (백혈병/골수 형성 이상 증후군)은 불루버드 뿐만 아니라 유전자 치료제 분야 전체에 큰 영향을 미쳤다. 특히 렌티바이러스 벡터를 이용한 유전자 치료제를 개발중이던 AVROBIO (AVRO), Orchard Therapeutics (ORTX), Rocket Pharmaceuticals (RCKT) 등의 기업들 역시 20~40%씩 폭락했다. 불루버드는 현재 1. 렌티바이러스의 염색체 삽입 부위로 인한 발병 2. 프리컨디셔닝에 사용된 busulfan에 의한 부작용 (프리컨디셔닝이란 골수 이식 투여 전 골수 이식이 용이하도록 환자의 골수에 존재하는 조혈 모세포를 제거하는 과정이다. ide-cel은 골수이식은 아니지만 투여 전 프리컨디셔닝으로 면역 세포 수를 줄여준다. busulfan은 골수 형성에 이상을 일으키는 부작용이 알려져있다) 3. 치료와는 무관한 발병으로 나눠 발병 원인을 조사 중이다. 최악의 경우는 렌티바이러스의 염색체 삽입으로 인한 발병으로 이 경우 유전 질환 파이프라인 전체가 무효화되면서 기업의 명운이 위태로워질 수도 있다.
2. 경쟁: 불루버드의 상용화를 앞둔 파이프라인들은 모두 first-in-class다. 그러나 best-in-class는 아니다. 더 뛰어난 효능을 지닌 후속 주자들이 등장했기 때문이다. SCD, TDT에 대한 유전자 치료제(불루버드 beti-cel)는 크리스퍼 테라퓨틱스가 버텍스 파마슈티컬즈와 공동으로 크리스퍼 유전자 가위를 이용한 세포 치료제 CTX001을 개발 중이다. 아직 초기 단계이지만 뛰어난 효능을 보여주고 있으며 beti-cel과 다른 메카니즘으로 염색체 무작위 삽입으로 인한 부작용 우려도 적다. 항암제 BCMA CAR-T (불루버드 ide-cel)의 경우 중국의 레전드 바이오테크와 J&J가 공동으로 개발중인 JNJ-4528/LCAR-B38M가 100%에 가까운 반응율을 보이며 뒤쫓아오고 있다.
3. 까다로와진 규제 당국: 유전자 치료, 세포 치료 분야는 비교적 최근에 개발되기 시작한 분야다. 아직 승인받은 치료제가 많지 않고 기존 저분자 화합물, 항체 치료제 등과는 비교도 되지 않을 정도로 복잡한 치료제이기 때문에 규제 당국의 가이드라인 역시 함께 만들어가는 중이다. 후기 임상시험에 돌입한 유전자 치료, 세포 치료제 후보물질들이 증가하고 FDA 승인 심사도 증가하면서 FDA는 지난해 부쩍 까다로운 조건들을 내걸기 시작했다. 일례로 큰 기대를 모으던 바이오마린 파마슈티컬즈의 혈우병 유전자 치료제가 올해 초 승인 거부됐고, 제조 공정에 대한 추가 서류 요구, 투여 기구에 대한 추가 실험 요구, 시험관에서의 효능 입증 실험 요구 등 다양한 사유로 여러 기업들의 FDA 승인 신청이 지연되고 있으며, 다수의 임상시험들이 임상 중단 명령을 받았다. 불루버드 역시 여러 차례 FDA 승인 신청이 지연된 바 있어서 올해 예정된 승인 신청이 예정된 스케쥴대로 진행되는지 지켜봐야한다.
불루버드에 대한 월가의 3월 투자 의견은 총 18건. 이중 적극 매수 5건, 매수 7건, 보유 5건, 매도 1건, 평균 점수 2.5로 약한 매수 의견이다. 평균 목표 주가는 $46.53로 현재 주가 대비% 상승 여력이 있다. 악재가 상당 부분 반영되어 있는 주가인 만큼 위험/보상 비율로 보았을 때 보상이 더 높다고 볼 수 있다. 하지만 3년 동안 내리 하락만 한 주식인 만큼 시장의 좋지 않은 센티먼트가 바뀔 때까지는 시간이 걸릴 수 있으며 3월 27일로 예정된 ide-cel의 승인 거부 혹은 승인 지연 시 주가는 추가로 하락할 가능성도 열려 있다. 변동성을 감내할 수 있는 투자자라면 손실을 감당할 수 있는 범위 내에서 투자해 보는 것도 나쁘지 않은 선택일 수 있다.
'외부 기고글' 카테고리의 다른 글
| 미용 시술용 의료 기기의 떠오르는 강자 InMode (0) | 2022.09.11 |
|---|---|
| 황제 등극을 앞둔 키트루다, 그리고 머크 (0) | 2022.09.11 |
| GW를 품에 안고 카나비스 시장으로, Jazz Pharmaceuticals (0) | 2022.09.11 |
| 유럽의 항체 플랫폼 강자 Genmab A/S (0) | 2022.09.11 |
| 뒤쳐진 백신 개발, 전화 위복의 계기가 될 것인가? Novavax (0) | 2022.09.11 |
