오늘 아침 제약-바이오 주요 소식 20201207 (feat ASH20)
미국 시간 2020년 12월 7일 월요일 장시작전 제약/바이오 주요 소식입니다. ASH20 첫 이틀 발표도 함께 다뤘습니다.
오늘따라 안그래도 ASH 발표양도 너무 많은데 일반 발표까지도 쏟아져서 정리하는데 좀 애먹었습니다. ASH는 너무 발표양이 많아서 눈에 띄는 것들만 담아봤습니다. 중요한 발표였지만 제가 놓친것도 많이 있을거라 봅니다.
첫 이틀간 ASH의 특징은 (1) 크리스퍼 유전자 가위 기술의 첫 유의미한 임상 결과 (2) 경쟁이 극한에 다르고 있는 BCMA 타게팅 필드에서 대략 효능은 CAR-T > 이중항체 > ADC로, 안전성은 반대 순서로 정도인 듯 합니다.
제약-바이오 일반
▼ Lipocine Inc. (NASDAQ:LPCN): FDA가 테스토스테론 저하증 남성에 대한 Tlando의 승인 심사를 12/7 주간에 하겠다고 통보. 원래 PDUFA는 11/30.
▼ Syros Pharmaceuticals (NASDAQ:SYRS): Orsenix로부터 SY-2101 (이전명 ORH-2014) 관련 자산을 $12M 선수금, $6M 승인 마일스톤, $10M 매출 마일스톤에 인수. SY-2101은 경구용 급성 전골수성 백혈병 (acute promyelocytic leukemia) 치료제 후보물질.
▼ Bayer (OTCPK:BAYZF), Atara Biotherapeutics (NASDAQ:ATRA): Bayer가 Atara의 고형암에 대한 off-the-shelf CAR-T ATA3271와 자가 CAR-T ATA2271를 라이선싱. 두 CAR-T 모두 mesothelin 타게팅. 선수금 $60M, 마일스톤 $610M.
▼ Chimerix (NASDAQ:CMRX): FDA가 천연두에 대한 brincidorfovir (BCV)의 승인 심사 Priority Review로 개시. PDUFA 2021-4-7.
▼ Sol Gel Technologies Ltd (NASDAQ: SLGL): FDA가 여드름에 대한 Twyneo의 승인 심사 개시. PDUFA 2021-8-1
▼ BioCryst Pharmaceuticals (NASDAQ:BCRX), Royalty Pharma (NASDAQ:RPRX): BioCryst가 Royalty Pharma와 Athyrium Capital Management LP로부터 지난주 FDA 승인 받은 ORLADEYO™ (berotralstat)의 출시를 위한 $325M의 자금 지원 받음.
▼ Xencor (NASDAQ:XNCR), Johnson & Johnson (JNJ): Janssen이 Xencor의 XmAb 이중항체 기술을 이용해 CD28과 공개되지 않은 전립선암 타겟에 대한 이중항체 개발 공동개발/라이선싱 딜. 선수금 $50M.
▼ Aligos Therapeutics (NASDAQ:ALGS), Merck (NYSE:MRK): Merck가 NASH 치료제 개발을 위해 Aligos의 올리고핵산 플랫폼 기술을 선수금과 최대 $458M 마일스톤에 라이선싱.
▼ scPharmaceuticals (NASDAQ:SCPH): FDA가 심부전에 대한 Furoscix (furosemide)의 승인 거부. 두번째 CRL. 거부 사유는 코로나-19로 인한 생산시설 점검 불가, 의약품을 구성하는 약물 이외 물품들에 대한 의문.
▼ Bellicum Pharmaceuticals (NASDAQ:BLCM): FDA가 사망환자 발생 후 췌장암, 전립선암에 대한 GoCAR-T 후보물질 BPX-601의 임상 1/2상에 대해 임상 중단 명령.
▼ Tonix Pharmaceuticals (NASDAQ:TNXP): 섬유근통(fibromyalgia)에 대한 TNX-102 SL (cyclobenzaprine HCl sublingual tablets)의 임상 3상에서 primary 및 주요 secondary endpoints 충족.
▼ Nabriva Therapeutics (NASDAQ:NBRV): Xenleta의 중국 유통을 위한 Sinovant Sciences와의 라이선스 계약 유리한 방향으로 개정.
▼ Lyra Therapeutics (NASDAQ:LYRA): 만성 축농증에 대한 LYR-210의 임상 2상이 통계적 유의미성 확보 실패.
▼ Daré Bioscience (DARE): 세균성 질염에 대한 DARE-BV1의 임상 3상에서 primary 및 secondary endpoints 충족. 그러나 부작용이 심하게 나옴.
▼ Sarepta Therapeutics (SRPT): Exon 51 skipping 돌연변이 듀켄근이영양증에 대한 SRP-5051의 임상 2상 MOMENTUM 결과 발표. eteplirsen (Exondys 51) 보다 10배 낮은 농도에서 효능 확인.
ASH20
▼ CRISPR Therapeutics (NASDAQ:CRSP), Vertex Pharmaceuticals (NASDAQ:VRTX): ASH 학회에서 지중해빈혈(TDT), 겸상적혈구증(SCD)에 대한 CRISPR/Cas9을 이용한 유전자 치료제 후보물질 CTX001의 임상 1/2상 CLIMB-111과 CLIMB-121의 결과 발표. CTX001를 투여한 10명의 환자들에서 지속적인 치료 효과 확인. 또한 각 임상시험의 첫번째 투여 환자에 대한 결과를 의학전문지 NEJM에 게재.
총 13명의 투여 환자들 중 투여후 3개월 이상이 된 7명의 TDT 환자에서 추적기간 3~18개월동안 수혈이 필요없었고 헤모글로빈 수치는 9.7~14.1 g/dL, 태아 헤모글로빈 (fetal hemoglobin) 40.9%~97.7%를 보임. 투여 6개월, 12개월된 환자 각 한명씩의 골수 유전자 분석에서 편집된 유전자가 유지고 있음을 확인. 한명의 치료 연관 부작용 포함 4건의 심각한 부작용이 관찰됐으나 보편적인 자가 줄기세포 이식에서 나타나는 부작용과 유사한 수준이며 치료 가능.
총 6명의 투여 환자들 중 투여후 3개월이 지난 3명의 SCD 환자들에서 추적기간 3~15개월간 혈관막힘위기 (vaso-occlusive crises, VOC)가 나타나지 않음. 헤모글로빈 수치 11.5~13.2 g/dL, 태아 헤모글로빈 (fetal hemoglobin) 31.3%~48.0%를 보임. 투여 6개월, 12개월된 환자 각 한명씩의 골수 유전자 분석에서 편집된 유전자가 유지고 있음을 확인. 심각한 부작용은 관찰되지 않았고 보편적인 자가 줄기세포 이식에서 나타나는 부작용과 유사한 수준의 부작용들이 관찰됐으며 치료 가능.
▼ bluebird bio, Inc. (Nasdaq: BLUE): 지중해빈혈에 대한 betibeglogene autotemcel (beti-cel, 이전명 LentiGlobin)의 장기 추적 확장 임상시험 LTF-303의 결과 및 유소년 대상 임상 3상 HGB-207 (Northstar-2)과 HGB-212 (Northstar-3) 결과 발표. 32명의 LTF-303 환자들 에서 64% (14/22)의 임상 1/2상 환자와 90% (9/10)의 임상 3상 환자가 수혈 불필요 (중위값 39.4개월, 19.4~69.4개월). 수혈 불필요 환자 헤모글로빈 수치는 임상 1/2상 환자 10.4 (9.4-13.3) g/dL, 임상 3상 환자 12.5 (11.9-13.5) g/dL. 외부 주입 헤모글로빈 유전자 (HbA T87Q) 수치는 임상 1/2상 환자의 경우 60개월까지 감소 없이 유지. 18세 이하 유소년 환자에 대한 임상 3상에서 중위 추적기간 14.9개월에 87% (13/15)가 수혈 불필요, 헤모글로빈 수치 11.3 (9.4-12.8) g/dL.
▼ Bristol Myers Squibb (NYSE: BMY), bluebird bio, Inc. (Nasdaq: BLUE): 재발성/불응성 다발성 골수종(RRMM)에 대한 idecabtagene vicleucel (ide-cel, BCMA CAR-T)의 임상 1상 CRB-401 결과 발표. ORR 76%, CR 39%, mDoR 10.3개월, mPFS 8.8개월, mOS 34.2개월 (중위 추적기간 14.7개월). 3등급 이상 CRS 7%, 4, 5등급은 없음. RRMM에 대한 ide-cel의 임상 2상 KarMMa의 하위그룹 분석 결과도 발표. 3차 이상 치료후 예후가 안좋은 그룹 ORR과 CR 각각 65% 이상, 20% 이상, mDoR 9.2개월 이상, mPFS 7.5개월 이상. 65세 및 70세 이상 그룹에서 ORR 84%~90%, CR 31%~35%, mDoR 10.7~11개월, mPFS 8.6~10.2개월. RRMM에 대한 bb21217의 임상 1상 CRB-402의 결과도 발표. bb21217은 ide-cel과 동일한 CAR-T세포를 배양조건을 바꿔 기억 T세포가 많이 생성되도록 한 치료제 후보물질.
▼ Legend Biotech Corporation (NASDAQ: LEGN), Johnson & Johnson (JNJ): 재발성/불응성 다발성 골수종(RRMM)에 대한 ciltacabtagene autoleucel (cilta-cel, BCMA CAR-T)의 임상 1b/2상 CARTITUDE-1 결과 발표. 중위 추적기간 12.4개월차 ORR 97%, CR 67%. 그러나 96명중 3명이 치료로 인한 부작용으로 사망.
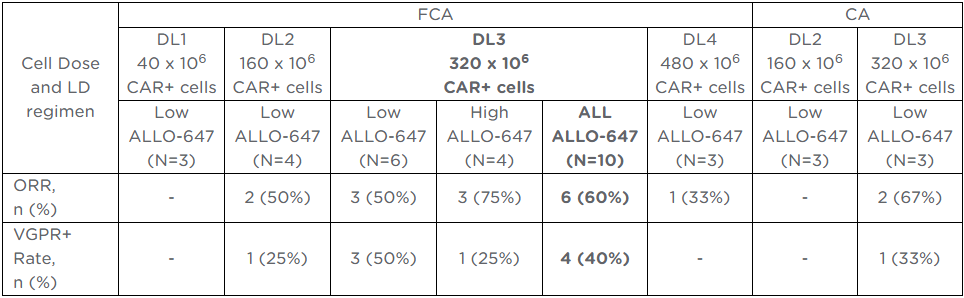
▼ Allogene Therapeutics, Inc. (Nasdaq: ALLO): 재발성/불응성 다발성 골수종(RRMM)에 대한 ALLO-715 (off-the-shelf CD52 CAR-T)의 UNIVERSAL 임상시험 결과 발표.
▼ Amgen (NASDAQ:AMGN): 재발성/불응성 다발성 골수종(RRMM)에 대한 AMG 701 (BCMA BiTE)의 용량 증가 임상 1상 결과 발표. AMG 701은 반감기를 늘린 BiTE 이중항체. 최소 3차 이상, 중위 치료 차수 6차의 환자 대상 3-18mg의 ORR 36%, 최고용량군 83%. 3등급 이상 CRS 9%.
▼ Regeneron Pharmaceuticals, Inc. (NASDAQ: REGN): 재발성/불응성 다발성 골수종(RRMM)에 대한 REGN5458 (BCMAxCD3 이중항체)의 임상 1/2상의 임상 1상 파트 결과 발표. 중위 치료 차수 5차. 용량별 결과는 아래 표 참조.

▼ Fate Therapeutics (NASDAQ:FATE): 재발성/불응성 B세포 림프종에 대한 off-the-shelf NK세포 치료제 후보물질 FT516과 rituximab (Rituxan, Roche) 병용의 임상 1상 중간 결과 발표. 4명 중 1명 PR, 2명 CR.
▼ Cellectis (Nasdaq: CLLS): B세포 급성 림프구성 백혈병 (B-ALL)에 대한 UCART22 (CD22 off-the-shelf CAR-T)의 용량증가 임상 1상 BALLI-01의 결과 발표. 용량 레벨1 두명 중 한명은 CRi, 한명은 CR. 치료로 인한 3등급 이상 부작용 없음.
▼ IGM Biosciences, Inc. (Nasdaq: IGMS): B세포 비호지킨 림프종에 대한 IGM-2323 (CD20 x CD3 IgM 이중항체)의 용량 증가 임상 1상 결과 발표. PR 2/14. 데이터 컷오프 후 최고용량 투여군 2명은 CR로.
▼ Xencor, Inc. (NASDAQ:XNCR): 재발성/불응성 급성 골수성 백혈병에 대한 vibecotamab (XmAb®14045, CD123 x CD3 이중항체)의 용량 증가 임상 1상 결과 발표. 중위 치료 차수 3차, 0.75 mcg/kg 이상 도즈 5사이클 이상 투여 54명의 환자에서 ORR 15% (8/54), CR 2명, 불완전한 혈액학적 회복 CR 3명. 3등급 이상 CRS 9% (10명).
▼ Constellation Pharmaceuticals (NASDAQ:CNST): 골수섬유증 (myelofibrosis, MF)에 대한 CPI-0610의 임상 2상 MANIFEST, 3상 MANIFEST-2 결과 발표. Ruxolitinib (Jakafi, Incyte)과의 병용 1차 치료 환자군 Arm 3에서 primary endpoint인 24주차 SVR35 (35% 이상 비장 크기 감소) 67% (42/63). 중위 비장 크기 감소 50%. 24주차 TSS50 57% (34/60). 중위 TSS 감소 59%. 2차 이상 CPI-0610 단독치료 환자군 Arm 1에서 24주차 SVR35 30% (7/23), TSS50 48% (10/21). Ruxolitinib 병용 2차 이상 치료 Arm 2에서 24주차 SVR35 29% (6/21), TSS50 38% (8/21). CPI-0610는 BET 저해제.
▼ Gilead Company (NASDAQ:GILD):
- Yescarta (axicabtagene ciloleucel)의 ZUMA-12, ZUMA-5 임상 2상 중간 결과 발표.
| 적응증 | 임상시험 | N | 중위추적기간 | ORR | CR |
| 고위험 큰 B세포 림프종 (large B-cell lymphoma, LBCL) 1차 치료 | 2상 ZUMA-12 | 27 | 9.3개월 | 85% | 74% |
| 나태한 비호지킨 림프종 (indolent non-Hodgkin lymphoma) 3차 치료 | 2상 ZUMA-5 | 104 | 17.5개월 | 92% | 76% |
| 여포성 림프종 (follicular lymphoma, FL) | 2상 ZUMA-5 | 84 | 17.5개월 | 94% | 80% |
| 주변 영역 림프종 (marginal zone lymphoma, MZL) | 2상 ZUMA-5 | 20 | 85% | 60% |
- 외투세포림프종 (mantle cell lymphoma, MCL)에 대한 Tecartus™ (brexucabtagene autoleucel, 이전명 KTE-X19)의 pivotal ZUMA-2 임상시험 결과 발표.
| 적응증 | 임상시험 | N | 중위추적기간 | ORR | CR |
| 외투세포림프종 (mantle cell lymphoma, MCL) | 2상 ZUMA-2 | 60 | 17.5개월 | 92% | 67% |
- 급성 백혈병에 대한 magrolimab (anto-CD47), azacitidine 병용 1차 치료 임상 1b상 업데이트 결과 발표.
| N | 중위추적기간 | ORR | CR | mDoR | mOS | |
| 전체 환자군 | 43 | 12.5개월 | 63% | 42% | 9.6개월 | 18.9개월 |
| TP53 돌연변이 환자군 | 29 | 4.7개월 | 69% | 45% | 7.6개월 | 12.9개월 |
▼ ALX Oncology Holdings Inc (Nasdaq: ALXO): NHL에 대한 ALX148 (CD47 저해제)의 임상 1상에서 고용량 투여군에서 ORR 70%
▼ Pfizer (NYSE:PFE), Sangamo Therapeutics (NASDAQ:SGMO): 혈우병 A에 대한 Factor VIII 유전자 치료제 후보물질 giroctocogene fitelparvovec (SB-525/PF-07055480)의 임상 1/2상 Alta의 추적 결과 발표. 고용량 그룹 (3 x 10^13 vg/kg)의 5명 모두 추적기간 1년 초과. 그룹 중위 FVIII 활성 56.9%, 그룹 FVIII 기하 평균 활성 70.4%. 5명 모두 투여 9주차부터 1년까지 출혈 없음. 한명이 52주 이후 한건의 출혈 발생.
▼ Aptose Biosciences (NASDAQ:APTO): CLL/NHL에 대한 CG-806의 임상 1상 업데이트 발표. 암 크기가 줄어들었지만 OR은 없었음.
▼ Oncternal Therapeutics (NASDAQ:ONCT): 재발성/불응성 MCL에 대한 cirmtuzumab, ibrutinib (Ibrance, Pfizer) 병용의 임상 1/2상 CIRLL의 업데이트 중간 결과 발표. ORR 87%.
▼ Eli Lilly and Company (NYSE: LLY): BTK 저해제 치료 경험이 있는 CLL, SLL에 대한 LOXO-305(BTK 저해제)의 임상 1/2 BRUIN 결과 발표. ORR 62%, 10개월 이상 추적시 ORR 84%로 증가.
▼ TG Therapeutics, Inc. (NASDAQ: TGTX): CLL에 대한 U2 + Venetoclax (AbbVie) 3중 병용 임상 1/2상 ORR 100% (n=27), CR 41%; B세포 림프종에 대한 TG-1701, U2 병용 임상 2상 병용 ORR 74%, CR 22% (n=14)
▼ Celyad Oncology (NASDAQ:CYAD): 급성 백혈병 (AML), 골수형성 이상 증후군 (myelodysplastic syndrome, MDS)에 대한 NKG2DR 타게팅 CAR-T CYAD-01의 임상 1상 THINK 결과 업데이트. ORR 0%. 개발 중단; AML, MDS에 대한 NKG2DR 타게팅 CAR-T CYAD-02의 임상 1상 CYCLE-1 결과 발표. 5명의 MDS 환자 mCR (marrow CR) 3, SD 2, 2명의 AML 1 SD.
▼ Sunesis Pharmaceuticals (NASDAQ:SNSS): 인수합병에 합의한 Viracta Therapeutics가 EBV 양성 림프종에 대한 nanatinostat, valganciclovir의 임상 2상에서 ORR 80%, CR 40% (n=10).
코로나-19
[어제 장중 or 아침에 놓친 것]
▼ Pfizer (PFE), BioNTech (BNTX): 영국에 이어 바레인에서 코로나-19 백신 BNT162b2를 긴급사용허가. 바레인은 중국 Sinopharm의 백신 역시 이미 긴급사용허가했음.
[어제 장마감후/오늘 장전]
▼ Matinas BioPharma (NYSEMKT:MTNB), Gilead Sciences (NASDAQ:GILD): NIAID가 렘데시비어의 경구용 제제를 전임상에서 테스트한다고 발표. 렘데시비어 경구용 제제는 Matinas BioPharma의 지질나노크리스탈 (lipid nanocrystal, LNC)을 사용.
▼ Moderna (MRNA): 캐나다가 40M 도즈에 대한 추가 구매 옵션 행사.
'Weekly Biotech Review > Daily Review' 카테고리의 다른 글
| 오늘 아침 제약-바이오 주요 소식 20201209 (feat ASH20) (1) | 2020.12.10 |
|---|---|
| 오늘 아침 제약-바이오 주요 소식 20201208 (feat ASH20) (0) | 2020.12.09 |
| 오늘 아침 제약-바이오 주요 소식 20201204 (0) | 2020.12.05 |
| 오늘 아침 제약-바이오 주요 소식 20201203 (2) | 2020.12.04 |
| 오늘 아침 제약-바이오 주요 소식 20201202 (0) | 2020.12.03 |
